|
| |
 |
 |
 |
| |
|
Aktive schubförmige Multiple Sklerose
6-Jahres-Daten bestätigen anhaltende Wirksamkeit und Sicherheit von Ofatumumab
|
|
| |
| |
In der Behandlung der aktiven schubförmigen Multiplen Sklerose
(relapsing multiple sclerosis; RMS) zeigte der monatlich subkutan (s.
c.) zu applizierendea, b, c Anti-CD20-Antikörper Ofatumumabd
in den beiden Zulassungsstudien ASCLEPIOS I und II gegenüber der
bisherigen Basistherapie mit Teriflunomid eine überlegene Wirksamkeit
bei vergleichbarer Sicherheit und Verträglichkeit [1]. Aktuelle
Ergebnisse einer Subgruppenanalyse (n=465) der offenen
Verlängerungsstudie ALITHIOS bestätigen für kürzlich diagnostiziertee,
therapienaive Patient*innen die anhaltend hohe Wirksamkeit und das
günstige Nutzen-Risiko-Profil von Ofatumumab für den
Beobachtungszeitraum von bis zu sechs Jahren [2, 3]. Der Großteil der
kürzlich diagnostiziertene, therapienaiven Patient*innen [3] erfüllte die Kriterien einer mild-aktivenf RMS. Für kürzlich diagnostiziertee,
therapienaive RMS-Patient*innen mit aktiver Erkrankung könnte ein
frühzeitiger Beginn der hochwirksamen Therapie (high efficacy therapy;
HETg) mit Ofatumumab von Vorteil sein [1, 3].
An der offenen Verlängerungsstudie ALITHIOS nahmen 1.367
Patient*innen teil, die die Zulassungsstudien ASCLEPIOS I und II beendet
hatten [2]. Davon wurden 677 von einer geringgradig wirksamen
krankheitsmodifizierenden Therapie (disease modifying therapy; DMT) mit
Teriflunomid auf eine HETg mit Ofatumumab (20 mg, s. c.) umgestellt, während 690 Patient*innen durchgehend Ofatumumab erhielten [2].
Subgruppenanalyse der kürzlich diagnostiziertene, therapienaiven RMS-Patient*innen
Ebenfalls analysiert wurden die Ergebnisse für die Subgruppe der kürzlich diagnostiziertene, therapienaiven Patient*innen [3]. Insgesamt 465 kürzlich diagnostiziertee,
therapienaive Patient*innen waren nach Ende der Zulassungsstudien
ASCLEPIOS I und II in die ALITHIOS-Studie eingeschlossen worden. Zum
Datenschnitt am 25. September 2023 führten 78,7 % (n=366) die
Behandlung mit Ofatumumab fort [3]. Davon hatten 181 Patient*innen
eine durchgängige Erstlinientherapie mit Ofatumumab erhalten
(OMB-Gruppe) und 185 waren in Jahr zwei bis drei von Teriflunomid auf
Ofatumumab umgestellt worden (TER-OMB-Gruppe) [3].
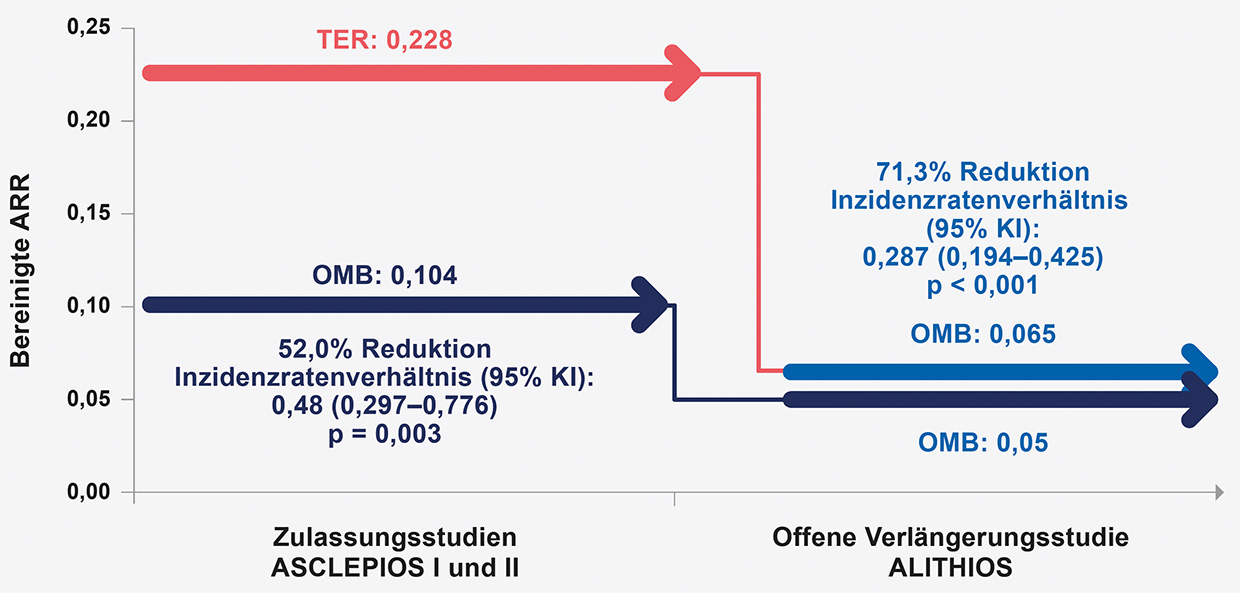
Reduktion der Schubrate: Etwa ein Schub alle 20 Jahre
Im Vergleich zur TER-OMB-Gruppe reduzierte die initiale Ofatumumab-Therapie bei den kürzlich diagnostiziertene,
therapienaiven Patient*innen über den Zeitraum von bis zu sechs
Jahren die Anzahl der bestätigten Schübe um 44 % [3]: Die
jährliche Schubrate (annualized relapse rate; ARR) blieb unter der
kontinuierlichen Behandlung mit Ofatumumab über einen
Beobachtungszeitraum von bis zu sechs Jahren konstant niedrig,
entsprechend etwa einem Schub alle 20 Jahre in der Verlängerungsphase
[3]. Die Umstellung von Teriflunomid auf Ofatumumab bei den kürzlich
diagnostiziertene, therapienaiven Patient*innen war mit einem Rückgang der ARR um 71,3 % (p<0,001) assoziiert (Abb. 1) [3].
|
|
| |
| |
 |
|
| |
Abb. 1: Reduktion der Schubrate (annualized relapse rate; ARR) bei kürzlich diagnostiziertene,
therapienaiven Patient*innen in den Zulassungsstudien ASCLEPIOS I und
II und der offenen Verlängerungsstudie ALITHIOS; mod. nach [3].
|
|
|
|
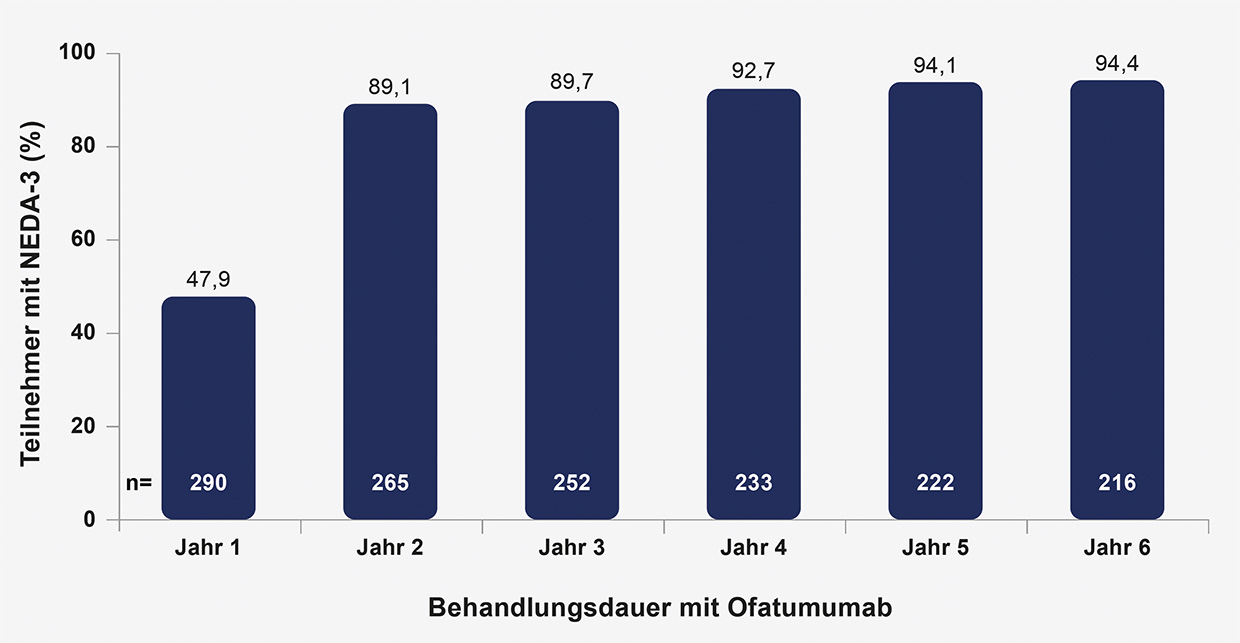
Stabile Unterdrückung der Krankheitsaktivität
Nach Beginn der Ofatumumab-Therapie stieg der Anteil an kürzlich diagnostiziertene,
therapienaiven Patient*innen, die die Kriterien NEDA-3 (no
evidence of disease activity-3: keine Schübe, Behinderungsprogression
oder MRT-Aktivität) erfüllten, schnell an. In Jahr sechs wiesen
94,4 % der Patient*innen, die durchgängig Ofatumumab erhielten,
keine Anzeichen von Krankheitsaktivität (NEDA-3) auf (Abb. 2) [3]. Die
Ergebnisse der Subgruppenanalyse für die kürzlich diagnostiziertene,
therapienaiven Patient*innen im Beobachtungszeitraum von bis zu sechs
Jahren stehen in Einklang mit den Daten für die gesamte
Studienpopulation [2, 3].
|
|
| |
 |
|
| |
Abb. 2: Anteil der kürzlich diagnostiziertene,
therapienaiven Patient*innen, die kontinuierlich Ofatumumab erhielten
und NEDA-3 Status erreichten (NEDA-3, no evidence of disease
activity/keine Anzeichen von Krankheitsaktivität); mod nach [3].
|
|
| |
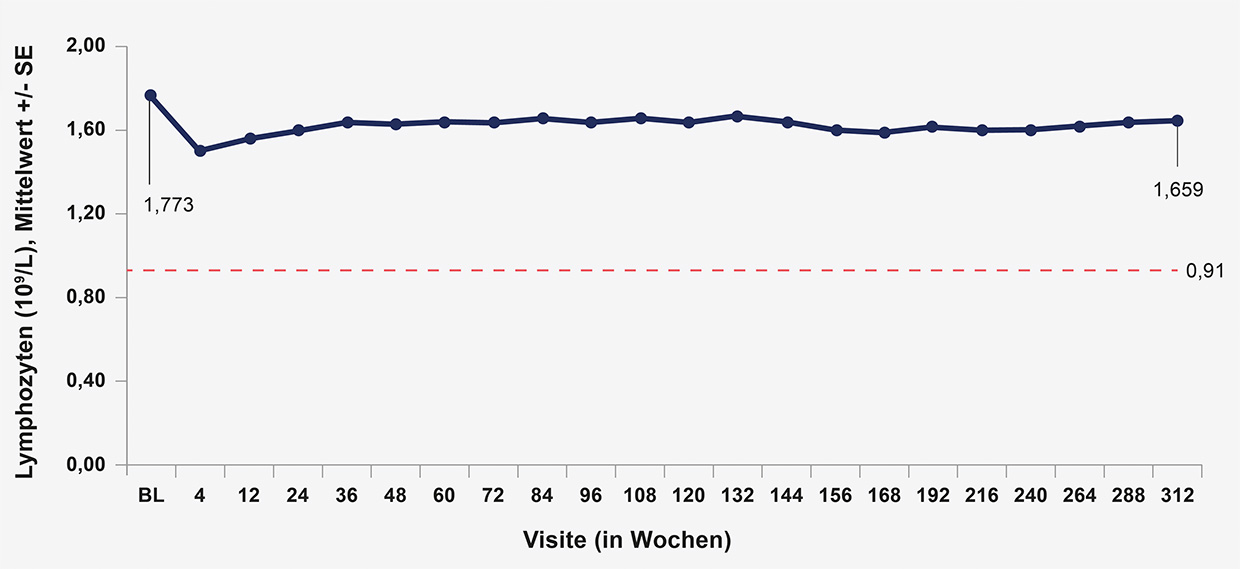
Erhalt der Immunkompetenz
Die mittleren IgG-Serumspiegel blieben in der Gesamtpopulation der
ALITHIOS-Studie im Beobachtungszeitraum von bis zu sechs Jahren in der
Ofatumumab-Therapiegruppe kontinuierlich stabil im Normbereich [2]. Die
Lymphozytenzahlen stiegen in der Ofatumumab-Gruppe nach einem kurzen
Abfall nach vier Wochen rasch wieder auf das Niveau bei Baseline und
blieben im Beobachtungszeitraum von bis zu sechs Jahren konstant (Abb.
3) [2].
|
|
| |
 |
|
| |
Abb. 3: Lymphozytenzahlen unter kontinuierlicher Ofatumumab-Therapie (SE, Standardfehler); mod. nach [2].
|
|
| |
Fazit
In der offenen Verlängerungsstudie ALITHIOS zeigte die
Erstlinientherapie mit Ofatumumab über einen Beobachtungszeitraum von
bis zu sechs Jahren eine anhaltend hohe Wirksamkeit in der
Gesamtpopulation sowie in der Subgruppe der kürzlich diagnostiziertene,
therapienaiven Patient*innen [3]. In der Gesamtstudienpopulation
bestätigte sich das günstige Nutzen-Risiko-Profil von Ofatumumab über
einen Zeitraum bis zu sechs Jahren [2]. Die Daten unterstreichen den
positiven Effekt einer frühen HETg bei kürzlich diagnostiziertene, therapienaiven Patient*innen [3].
a Die Behandlung ist durch einen Arzt oder eine Ärztin mit Erfahrung in der Behandlung neurologischer Erkrankungen einzuleiten.
b Nach einer erfolgten Initialdosis in den Wochen 0, 1 und 2.
c Erst nach Schulung durch entsprechend geschultes medizinisches Fachpersonal.
d Ofatumumab ist zur Behandlung von erwachsenen
RMS-Patient*innen mit aktiver Erkrankung, definiert durch klinischen
Befund oder Bildgebung, zugelassen.
e kürzlich diagnostiziert: Behandlungsbeginn innerhalb von 3 Jahren nach Erstdiagnose.
f Mild-aktive RMS: Mild-aktive RMS ist eine Definition von
Novartis gemäß der durchschnittlichen Patient*innencharakteristika in
den ASCLEPIOS-Zulassungsstudien I und II [1].
g Analog [4] gemäß Wirksamkeitskategorie 3.
|
|
| |
 |
|
| |
|
|
| |
Referenzen:
|
|
| |
1. Hauser SL et al., N Engl J Med 2020, 383:546–557.
|
|
| |
2. Wiendl H et al., Jahrestagung der American Academy of Neurology (AAN), 13.–18. April 2024, Denver, CO/USA, Poster P9.010.
|
|
| |
3.
Pardo G et al., Jahrestagung der American Academy of Neurology
(AAN),13.–18. April 2024, Denver, CO/USA, Oral Presentation S31.003.
|
|
| |
4.
Deutsche Gesellschaft für Neurologie (DGN), S2k-Leitlinie: Diagnose und
Therapie der Multiplen Sklerose,
Neuromyelitis-optica-Spektrum-Erkrankungen und MOG-IgG assoziierten
Erkrankungen, Stand: 30.11.2023, AWMF-Registernummer 030/050.
|
|
| |
|
|
| |
|
|
| |
Die Pflichtangaben finden Sie unter: www.novartis.com/de-de/kesimpta
Novartis Pharma Vertriebs GmbH
Sophie-Germain-Straße 10
90443 Nürnberg
Deutschland
novartis.de
|
|
| |
 |
|
|
|
|
|
| |
|
|

|
„Ärztliche Praxis Neurologie und Psychiatrie“ ist ein Titel der Biermann Verlag GmbH in Köln. Sie erhalten diese E-Mail, da Sie für diesen Newsletter angemeldet sind. Sie können in unserem Fachportal weitere Newsletter zu verschiedenen medizinischen Fachrichtungen abonnieren. Sollten Sie kein Interesse mehr an diesem Newsletter haben, können Sie sich hier abmelden. Haben Sie Fragen oder Anregungen zu unseren Themen und Inhalten, freuen wir uns auf Ihre E-Mail: [email protected].
Bitte beachten Sie, dass dieser Newsletter nur Angehörigen der Heilberufe gemäß HWG §10 zugänglich gemacht werden darf; das gilt auch für das Weiterempfehlen und Weiterleiten. Impressum: Biermann Verlag GmbH | MedCon Health Contents GmbH | HRB Bonn 11110 | HRB Köln 78926
Geschäftsführer: Dr. med. Hans Biermann
Hier vollständiges Impressum aufrufen
|
|
|
|
|
|