![Haut und Juckreiz optimal unter Kontrolle§ für mehr Lebensqualität [1,2]](https://biermann-medizin.de/content/uploads/2025/02/NL_OK_Header_1300px-1.png)
|
|
Haut und Juckreiz optimal unter Kontrolle§ für mehr Lebensqualität1,2
|
|
|
|
Liebe Leserinnen und Leser,
atopische Dermatitis ist eine Erkrankung, die für Betroffene oft eine große physische und auch mentale Belastung darstellt.3 Schenken Sie Ihren AD-Patient*innen eine Verbesserung der Lebensqualität, indem Sie mit der RINVOQ®-Therapie$4 gleich zwei optimale Ziele erreichen:1
|
|
|

|
|
|
Durch das gleichzeitige Anstreben von nahezu keinen Hautläsionen und fast keinem Juckreiz, können Sie bei Ihren Patient*innen eine optimale Krankheitskontrolle erreichen, die für Sie sichtbar, für Ihre Patient*innen spürbar ist1,2.
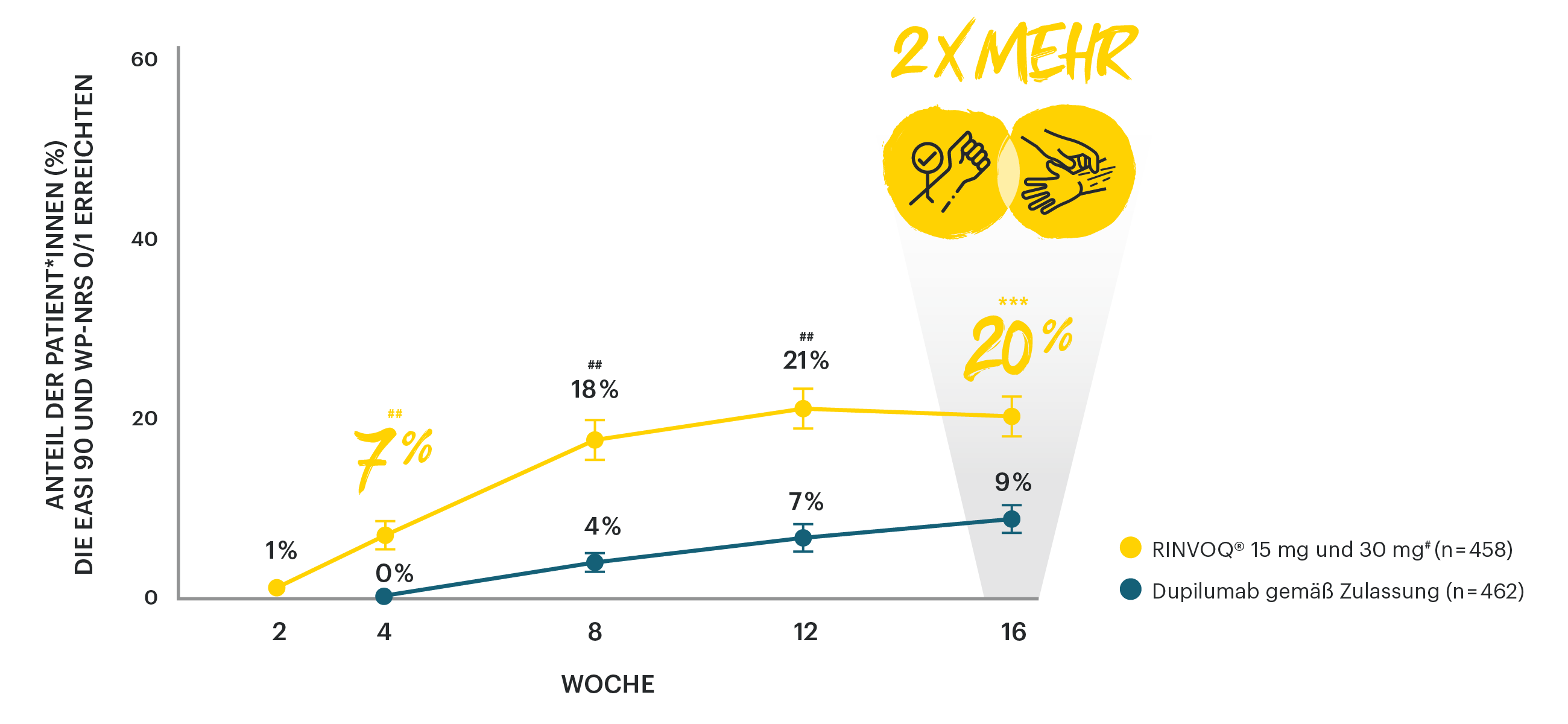
Optimale Krankheitskontrolle mit RINVOQ®5
|
|
|
|
|
| |
Bei AD-Patient*innen von denen knapp 60% mittelschwer betroffen sind, zeigt sich unter RINVOQ®-Therapie eine eindeutige Überlegenheit zu Dupilumab: Nach 16 Wochen erreichten im Vergleich zu Dupilumab doppelt so viele Patient*innen eine optimale Krankheitskontrolle definiert als das gleichzeitige Erreichen von zwei optimalen Zielen: Z.B. nahezu keine Hautläsionen (EASI 90) und fast keinen Juckreiz (WP-NRS 0/1).5 Im Praxisalltag erreichten unter RINVOQ® 49% der Patient*innen nach einem Jahr einen DLQI 0/1, womit sich zeigt: Mit RINVOQ® können Sie eine schnelle und langanhaltende Krankheitskontrolle erreichen.6
Überzeugen Sie sich selbst und schenken Sie Ihren AD-Patient*innen eine ganz neue Lebensqualität!
|
|
|

|
|
|
|
|
| |
$ Zugelassen zur Behandlung von mittelschwerer bis schwerer atopischer Dermatitis bei Erwachsenen und Jugendlichen ab 12 Jahren, die für eine Systemtherapie infrage kommen.4
§ Optimale Krankheitskontrolle ist definiert als minimale Krankheitsaktivitat (engl. Minimal Disease Activity, MDA). Diese beschreibt das gleichzeitige Erreichen von optimalen Therapiezielen eines objektiven Scores (z.B. EASI 90) und eines subjektiven Scores (z.B. WP-NRS 0/1).2
# Patientenindividuelle Dosisanpassung von 15 mg auf 30 mg QD möglich bei Patient*innen mit unzureichendem Ansprechen, wenn ab Woche 4 ein Ansprechen < EASI 50, oder ab Woche 4 eine Juckreizverbesserung ΔWP-NRS < 4 oder ab Woche 8 ein Ansprechen < EASI 75 festgestellt wurde.5
*** p < 0,0001; multiplizitätskontrolliert.
## p < 0,001; nominal. Nominale p-Werte zeigen statistische Unterschiede zwischen den Behandlungsgruppen für Endpunkte, die nicht auf Multiplikation kontrolliert wurden. Daher können aus diesen p-Werten keine endgültigen klinischen Schlussfolgerungen gezogen werden.
1 Reich K et al., J Eur Acad Dermatol Venereol. 2023; 37:1634–1641.
2 Silverberg JI et al., J Eur Acad Dermatol Venereol. 2004; 38(11):2139-2148.
3 Ring J et al., Eur Acad Dermatol Venereol. 2019; 33(7):1331–1340.
4 RINVOQ® Fachinformation, aktueller Stand.
5 Silverberg JI et al., Br J Dermatol 2025; 192:36–45.
6 Weidinger S et al., Real-World Effectiveness of Upadacitinib on Atopic Dermatitis Severity and Hard-To-Treat Localizations: One-Year Results from the German Observational Study UP-TAINED. EADV Spring Symposium 2024; Poster P689.
Rinvoq® 15 mg / 30 mg / 45 mg Retardtabletten;
Wirkstoff: Upadacitinib
Zusammensetzung: : 1 Rinvoq 15 mg / 30 mg / 45 mg Retardtablette enthält Upadacitinib 0,5 H2O, entsprechend 15 mg / 30 mg / 45 mg Upadacitinib. Sonstige Bestandteile: Tablettenkern: Mikrokristalline Cellulose, Hypromellose, Mannitol, Weinsäure, Hochdisperses Siliciumdioxid, Magnesiumstearat; Filmüberzug: Poly(vinylalkohol), Macrogol, Talkum, Titandioxid (E171), Eisen(III)-oxid (E172); nur in Rinvoq 15 mg: Eisen(II,III)-oxid (E172); nur in Rinvoq 45 mg: Eisen(III)-hydroxid-oxid x H2O (E172). Anwendung: Rinvoq 15 mg: Mittelschwere bis schwere aktive rheumatoide Arthritis bei Erwachsenen, die auf ein oder mehrere krankheitsmodifizierende Antirheumatika (DMARDs) unzureichend angesprochen oder diese nicht vertragen haben (allein oder in Kombination mit Methotrexat (MTX)). Aktive Psoriasis-Arthritis bei Erwachsenen, die auf ein oder mehrere DMARDs unzureichend angesprochen oder diese nicht vertragen haben (allein oder in Kombination mit MTX). Aktive ankylosierende Spondylitis bei Erwachsenen, die auf eine konventionelle Therapie unzureichend angesprochen haben. Aktive nicht röntgenologische axiale Spondyloarthritis bei Erwachsenen mit objektiven Anzeichen einer Entzündung, angezeigt durch erhöhtes C‑reaktives Protein und/oder Nachweis durch Magnetresonanztomografie, die unzureichend auf NSAR angesprochen haben. Rinvoq 15 mg / 30 mg: Mittelschwere bis schwere atopische Dermatitis bei Erwachsenen und Jugendlichen ab 12 Jahren, die für eine systemische Therapie in Frage kommen. Rinvoq 15 mg / 30 mg / 45 mg: Mittelschwere bis schwere aktive Colitis ulcerosa bei Erwachsenen, die auf eine konventionelle Therapie oder ein Biologikum unzureichend angesprochen haben, nicht mehr darauf ansprechen oder diese nicht vertragen haben. Mittelschwerer bis schwerer aktiver Morbus Crohn bei Erwachsenen, die auf eine konventionelle Therapie oder ein Biologikum unzureichend angesprochen haben, nicht mehr darauf ansprechen oder diese nicht vertragen haben. Gegenanzeigen: Überempfindlichkeit gegen einen der Bestandteile; aktive Tuberkulose; aktive schwerwiegende Infektionen; schwere Leberinsuffizienz; Schwangerschaft. Nebenwirkungen: Infektionen der oberen Atemwege; Bronchitis; Herpes zoster; Herpes simplex; Follikulitis; Influenza; Harnwegsinfektion; Pneumonie; orale Candidose; Divertikulitis; Sepsis; nichtmelanozytärer Hautkrebs; Anämie; Neutropenie; Lymphopenie; Urtikaria; schwerwiegende Überempfindlichkeitsreaktionen; Hypercholesterinämie; Hyperlipidämie; Hypertriglyzeridämie; Kopfschmerzen; Schwindelgefühl; Drehschwindel; Husten; Bauchschmerzen; Übelkeit; gastrointestinale Perforation; Akne; Ausschlag; Fatigue; Fieber; CPK im Blut erhöht; ALT erhöht; AST erhöht; Gewicht erhöht; Zusätzliche Nebenwirkung bei Jugendlichen mit Atopischer Dermatitis: Hautpapillom.
Verschreibungspflichtig; Pharmazeutischer Unternehmer:
AbbVie Deutschland GmbH & Co. KG, Knollstraße, 67061 Ludwigshafen, Deutschland
Stand: Oktober 2024
|
|
|
|
|
|

|
„Kompakt Dermatologie und Allergologie“ ist ein Titel der Biermann Verlag GmbH in Köln. Sie erhalten diese E-Mail, da Sie für diesen Newsletter angemeldet sind. Sie können in unserem Fachportal weitere Newsletter zu verschiedenen medizinischen Fachrichtungen abonnieren. Sollten Sie kein Interesse mehr an diesem Newsletter haben, können Sie sich hier abmelden. Haben Sie Fragen oder Anregungen zu unseren Themen und Inhalten, freuen wir uns auf Ihre E-Mail: [email protected]. Bitte beachten Sie, dass dieser Newsletter nur Angehörigen der Heilberufe gemäß HWG §10 zugänglich gemacht werden darf; das gilt auch für das Weiterempfehlen und Weiterleiten.
Impressum: Biermann Verlag GmbH | MedCon Health Contents GmbH | HRB Bonn 11110 | HRB Köln 78926
Geschäftsführer: Dr. med. Hans Biermann
Hier vollständiges Impressum aufrufen
|
|
|
|
|
|