|
Liebe Leserinnen und Leser,
zur Behandlung des sekundären Hyperparathyreoidismus (sHPT) bei Erwachsenen mit chronischer Nierenerkrankung (CKD) im Stadium G3 oder G4 und Vitamin-D-Mangel steht mit RAYALDEE® (Extended-Release-Calcifediol) eine effektive Therapieoption zur Senkung des Parathormon-(PTH)-Spiegels zur Verfügung.1
Inwiefern können sHPT-Patient:innen von RAYALDEE® profitieren ?
|
|
|
|
|
Fallbericht zeigt Vorteile einer Umstellung auf RAYALDEE®
Ein 85-jähriger sHPT-Patient im CKD-Stadium G4 wurde als kardiovaskulärer Hochrisikopatient eingestuft. Aufgrund eines auffällig erhöhten PTH-Spiegels (104,8 ng/l; 11,1 pmol/l) bei 25-Hydroxyvitamin-D-Werten (25(OH)D) im unteren therapeutischen Zielbereich, erhielt er initial alle 2 Wochen natives Vitamin D (NVD, Cholecalciferol). Im Zeitraum von 1,5 Jahren stieg PTH weiterhin an, bei gleichzeitiger Absenkung von 25(OH)D (Abb. 1). Um eine weitere Progression des sHPT zu vermeiden, wurde ein Therapiewechsel auf RAYALDEE® vorgenommen.
Nach Umstellung auf RAYALDEE® (30µg/Tag) sank der PTH-Wert innerhalb von 2 Monaten, während 25(OH)D deutlich anstieg (Abb. 1). Nach 6 Monaten stabilisierten sich die PTH- und 25(OH)D-Spiegel, gleichzeitig blieben Serum-Kalzium und Serum-Phosphat über den gesamten Zeitraum im KDIGO-Referenzbereich.2
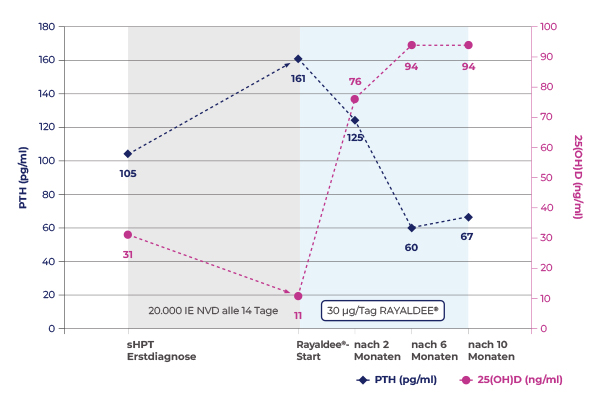
Abb. 1: Verlauf von PTH und 25(OH)D bei einem 85-jährigen sHPT-Patienten. Eigene Abbildung, data on file.
Weitere Details zum Fallbericht erfahren Sie hier.
|
|
|
|

|
Expertenempfehlungen für die Anwendung von RAYALDEE®
Auch die kürzlich in der NEPHRO-News veröffentlichten Expertenempfehlungen für die Anwendung von RAYALDEE® befürworteten bei vorbehandelten sHPT-Patient:innen mit PTH-Dynamik eine Umstellung auf RAYALDEE®. Dies gilt besonders bei einem 25(OH)D-Spiegel unter 30 ng/ml, mit Phosphat- und Calcium-Werten im Normalbereich (Abb. 2).3
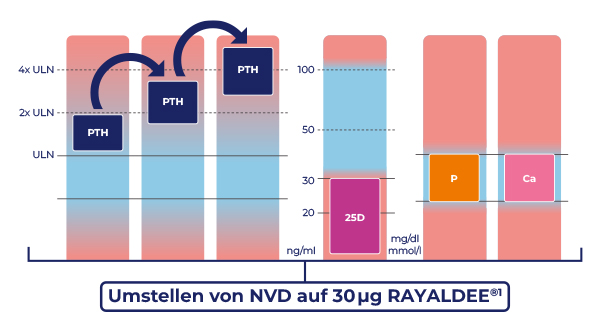
Abb. 2: Labordiagnostik bei vorbehandelten sHPT-Patient:innen mit PTH-Dynamik. Daten aus Kielstein et al. 2024.3
Eine deutsche Expertengruppe diskutierte die Pathophysiologie und Klinik des sHPT sowie dessen mögliche diätetische und pharmakologische Beeinflussung. Anhand von klinischen Praxiserfahrungen wurden spezifische Empfehlungen für die Anwendung von RAYALDEE® abgeleitet. Diese umfassen den Einsatz bei Erstvorstellung und bei Langzeitbehandlung von sHPT-Patient:innen, sowie weitere Empfehlungen zu Labordiagnostik, Therapieeinleitung und Verlaufskontrolle.3
Die Expert:innen betonen die Notwendigkeit einer frühzeitigen Diagnose und Therapie, um den sHPT zu verhindern oder zu kontrollieren, den Dialysestart hinauszuzögern und folgenschwere Komplikationen zu verhindern.
|
|
|
|
|
Besuchen Sie unsere Vifor Pharma PRO-Website und erfahren Sie mehr über RAYALDEE®!
|
|
|
|
|
Die aktuelle Fachinformation für Rayaldee® können Sie hier abrufen.
|
|
|
|
|
Abkürzungen:
25(OH)D = 25-Hydroxyvitamin D, Ca = Calcium, CKD = chronische Nierenerkrankung, ERC = Extended-Release Calcifediol, NVD = natives Vitamin D, P = Phosphat, PTH = Parathormon, sHPT = sekundärer Hyperparathyreoidismus.
Literatur:
- Rayaldee® (Calcifediol) Fachinformation, Stand Dezember 2022.
- London G, et al. Clin Nephrol 2010;74:423-32.
- Kielstein J, et al. NephroNews 2024;3.
|
|
|
|
| |
|
| |

|
|
Vifor Pharma Gruppe
Vifor Pharma Deutschland GmbH
Gmunder Straße 25
D-81379 München
Telefon +49 89 324 918 600
Fax +49 89 324 918 601
www.viforpharma.de
|
Vifor Pharma Deutschland GmbH und Fresenius Medical Care Nephrologica Deutschland GmbH sind Unternehmen der Vifor Pharma Gruppe.
Registergericht München: HRB 165582 / Ust. Id. Nr. DE 252256266 / Steuernummer 143/190/30698 / Geschäftsführer: Annegret Wittich-Höffer & Alexandros Sigalas
Registergericht Bad Homburg v.d.Höhe: HRB 10311 / Ust. Id. Nr. DE 249375071 / Steuernummer 003/233/68512 / Geschäftsführer: Annegret Wittich-Höffer & Marcus Gerhard Kracht
|
DE-RAY-2400061
RAYALDEE® 30 Mikrogramm, Weichkapsel retardiert. Wirkstoff: Calcifediol in Form von Calcifediolmonohydrat. Zusammensetzung: Eine retardierte Weichkapsel enthält 30 Mikrogramm Calcifediol in Form von Calcifediolmonohydrat. Wirkstoff: Calcifediol. Sonstige Bestandteile: Sorbitol (E420), Alkohol (Ethanol) Hartparaffin, Dünnflüssiges Paraffin, Hypromellose, Glycerolmonostearat, Macrogolglycerollaurate 32 (Ph.Eur.) Butylhydroxytoluol (Ph.Eur.). Hydroxypropylstärke, iota-Carrageen (Ph.Eur.), Dinatriumphosphat, Lösung von partiell dehydratisiertem Sorbitol (Ph.Eur.), Brillantblau FCF (E133), Titandioxid (E 171), gereinigtes Wasser. Anwendungsgebiete: Zur Behandlung des sekundären Hyperparathyreoidismus (sHPT) bei Erwachsenen mit chronischer Nierenerkrankung (chronic kidney disease, CKD) im Stadium 3 oder 4 und Vitamin-D-Mangel. Gegenanzeigen: Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile. Warnhinweise: Während der Behandlung mit Rayaldee® kann es zu einer Hypercalcämie kommen. Eine schwere Hypercalcämie kann eine Notfallbehandlung erforderlich machen. Hypercalcämie kann unabhängig von der Ursache das Risiko einer Digitalisintoxikation erhöhen. Eine vermehrte Phosphataufnahme in Verbindung mit der Einnahme von Vitamin-D-Präparaten kann zu einer Hyperphosphatämie führen. Patienten mit einer anamnestischen Hyperphosphatämie vor Einleitung der Therapie mit Rayaldee®, sollten während der Therapie häufiger auf eine mögliche Hyperphosphatämie kontrolliert werden. Eine adyname Osteopathie mit einem daraus resultierenden erhöhten Risiko für Frakturen kann sich entwickeln, wenn die Konzentrationen des intakten PTH über längere Zeit übermäßig unterdrückt werden. Die Dosierempfehlungen beziehen sich auf erwachsene Patienten mit nicht dialysepflichtiger chronischer Nierenerkrankung. Nebenwirkungen: Häufig (≥1/100, <1/10): erhöhtes Phosphat im Blut. Hypercalcämie. Verstopfung, Übelkeit, Diarrhoe. Gelegentlich (≥1/1.000, <1/100): verminderter Appetit. Abdominale Beschwerden, Mundtrockenheit, Erbrechen. Asthenie. Schwindelgefühl, Kopfschmerz. Verschreibungspflichtig. Bitte lesen Sie vor Verordnung von Rayaldee® die Fachinformation. Pharmazeutischer Unternehmer, Inhaber der Zulassung: Vifor Fresenius Medical Care Renal Pharma France, 100–101 Terrasse Boieldieu, Tour Franklin La Défense 8, 92042 Paris La Défense Cedex, Frankreich. Stand der Information: Oktober 2021.
|
|
|
|
|
„Kompakt Nephrologie“ ist ein Titel der Biermann Verlag GmbH in Köln. Sie erhalten diese E-Mail, da Sie für diesen Newsletter angemeldet sind. Sie können in unserem Fachportal weitere Newsletter zu verschiedenen medizinischen Fachrichtungen abonnieren. Sollten Sie kein Interesse mehr an diesem Newsletter haben, können Sie sich hier abmelden. Haben Sie Fragen oder Anregungen zu unseren Themen und Inhalten, freuen wir uns auf Ihre E-Mail: [email protected].
Bitte beachten Sie, dass dieser Newsletter nur Angehörigen der Heilberufe gemäß HWG §10 zugänglich gemacht werden darf; das gilt auch für das Weiterempfehlen und Weiterleiten. Impressum: Biermann Verlag GmbH | MedCon Health Contents GmbH | HRB Bonn 11110 | HRB Köln 78926
Geschäftsführer: Dr. med. Hans Biermann
Hier vollständiges Impressum aufrufen
|
|
|
|
|
|