|
Jetzt bei noch mehr Patienten einsetzbar
|
Liebe Leserinnen und Leser,
|
|
|
|
|
Bisher
|
|
war Kinpeygo® für erwachsene Patienten mit einer primären IgA-Nephropathie mit rascher Krankheitsprogression und einer UPCR
von ≥ 1,5 g/Gramm bedingt zugelassen.
|
|
Jetzt
|
|
hat die Europäische Kommission beschlossen:
|
|
Kinpeygo® ist zur Behandlung von Erwachsenen mit primärer
IgA-Nephropathie (IgAN) mit einer Proteinausscheidung im Urin von ≥ 1,0 g/Tag oder einer Protein/Kreatinin-Ratio im Urin (UPCR) von ≥ 0,8 g/Gramm zugelassen.1
|
|
Aufgrund der gesenkten Proteinurie-Verschreibungsgrenze kann Kinpeygo® eine größere Patientenpopulation adressieren und eine Therapie zu einem früheren Zeitpunkt der Erkrankung ermöglichen.1 Die Indikationserweiterung basiert auf den Ergebnissen von Teil B der zulassungsrelevanten Phase-III-Studie NefIgArd.2
|
|
|
|
|
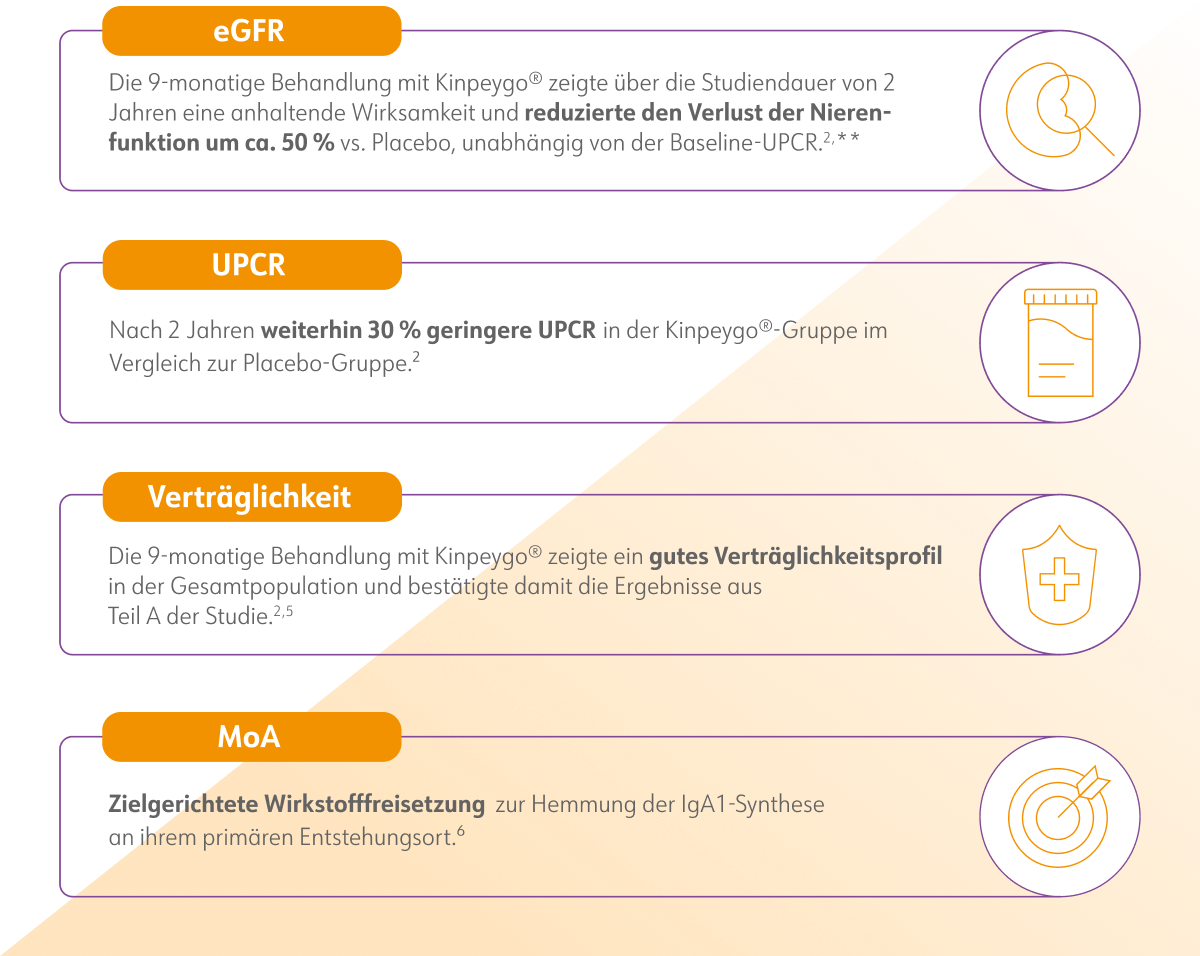
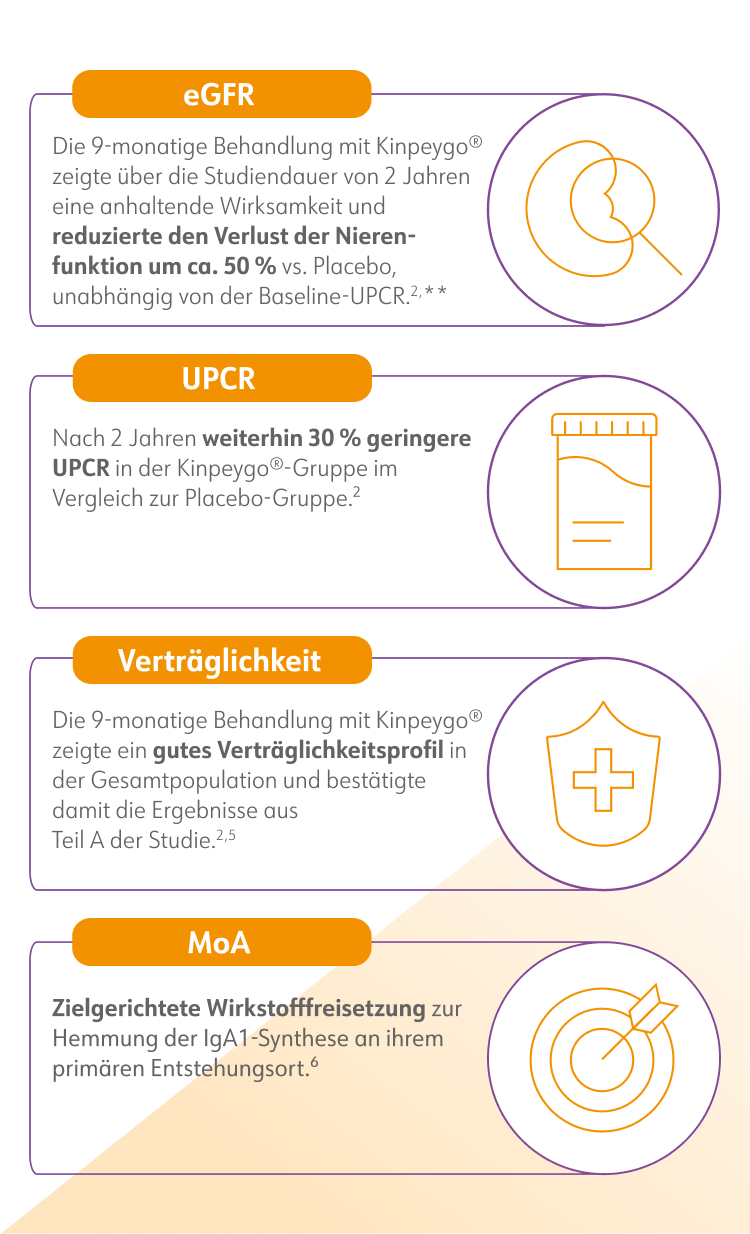
Die Studiendaten zeigen, dass die geschätzte glomeruläre Filtrationsrate (eGFR) nach der 9-monatigen Behandlung mit Kinpeygo® im Vergleich zum Ausgangswert stabil blieb (+0,66ml/min/1,73m2), während die Nieren-funktion in der Placebo-Gruppe signifikant abnahm (4,56ml/min/1,73m2). Dieser klinisch relevante Unterschied blieb auch im Beobachtungszeitraum von 15 Monaten nach Absetzen der Prüfmedikation und unter Fortführung der optimierten RAS-Blockade erhalten:2
Nach insgesamt 2 Jahren wurde der Verlust der Nierenfunktion um 50 % gegenüber Placebo reduziert.2
|
|
|
|
|
Diese Daten schließen die durch die Indikationserweiterung erschlossene Patientensubgruppe UPCR < 0,8 g/Gramm mit ein. Hier konnte gezeigt werden, dass auch bei einer UPCR < 0,8 g/Gramm die Progression der IgAN nach 24 Monaten verlangsamt werden konnte.3
In der EU ist Kinpeygo® die einzige zugelassene Therapie, die am Ursprung der IgA-Nephropathie ansetzt. Eine frühere Therapie der Erkrankung am Ort der Entstehung kann den Krankheitsverlauf modifizieren und den Verlust der Nephrone reduzieren. Dieser Effekt wiederum reduziert das Fortschreiten der CKD.4
|
|
|
|
|
Langzeiteffekte von Kinpeygo® im Überblick
|
 |
 |
|
Informieren Sie sich jetzt über die Teil B-Studiendaten, die Ihnen neue Möglichkeiten in der IgAN-Therapie mit Kinpeygo® eröffnen.
|
| Jetzt informieren |
|
|
|
|
|
|
|
Proteinausscheidung im Urin von ≥ 1,0 g⁄ Tag oder einer Protein⁄Kreatinin-Ratio im Urin (UPCR) von ≥ 0,8 g⁄Gramm
Kinpeygo® ist zur Behandlung von Erwachsenen mit primärer Immunglobulin A-Nephropathie (IgAN) mit einer Proteinausscheidung im Urin von ≥ 1,0 g/Tag (bzw. einer Protein/Kreatinin-Ratio im Urin von ≥ 0,8 g/Gramm) zugelassen.1
|
|
|
|
|
|
REFERENZEN:
|
-
Fachinformation Kinpeygo® 4 mg Hartkapseln mit veränderter Wirkstofffreisetzung, Stand 07/24.
-
Lafayette R et al. Efficacy and safety of a targeted-release formulation of budesonide in patients with primary IgA nephropathy (NefIgArd): 2-year results from a randomised phase 3 trial. Lancet 2023; 402(10405): 859–870 (inkl. ergänzendem Anhang).
-
Barratt J et al. Nefecon treatment provides kidney benefits for patients with IgAN that extend to those with low levels of UPCR: A subanalysis of the Phase 3 NefIgArd trial. WCN’24. Abstract: WCN24-1776.
-
Barratt J. 61th ERA Congress Stockholm; Vortrag CME 1 – Glomerulonephritis, Vasculitis, Autoimmune disease and Nephropathology. 23. Mai 2024.
-
Barratt J et al. Results from part A of the multi-center, double-blind, randomized, placebocontrolled NefIgArd trial evaluated targeted-release formulation of budesonide for the treatment of primary immunoglobulin A nephropathy. Kidney Int 2023; 103(2): 391–402 (inkl. ergänzendem Anhang).
-
Molyneux K et al. Treatment With Nefecon Reduces Circulating Levels of Galactose-Deficient IgA in Patients With IgA Nephropathy in the NefIgArd Clinical Trial. ASN kidney week 2022; Abstract: SA-PO654.
|
|
|
|
|
Kinpeygo® 4 mg Hartkapseln mit veränderter Wirkstofffreisetzung
Wirkstoff: Budesonid. Zus.: 1 Hartkaps. m. veränd. Wirkstofffreisetz. enth. 4 mg Budesonid. Sonst. Bestandt.: Zucker-Stärke-Pellets, Hypromellose, Macrogol, Citronensäure-Monohydrat, Ethylcellulose, mittelkett. Triglyceride, Ölsäure, Titandioxid (E171), Poly(methacrylsäure-co-methylmethacrylat), Talkum, Dibutyldecandioat, Schellack, Eisen(II,III)-oxid (E172). Anw.: Behandl. v. Erw. m. prim. Immunglobulin A-Nephropathie (IgAN) m. e. Proteinausscheid. i. Urin v. ≥ 1,0 g/Tag (bzw. e. Protein/Kreatinin-Ratio i. Urin v. ≥ 0,8 g/Gramm). Gegenanz.: Überempf. gg. d. Wirkst. od. e. d. sonst. Bestandt.; schwere Leberfunkt.stör. (Child-Pugh-Klasse C). Schwangersch./Stillz.: Nur nach sorgfält. Nutzen-Risiko-Abwäg. NW: Erhöh. Blutkörperchenzahl, erhöh. Neutrophilenzahl, Sympt. d. Cushing-Syndr., Diab. mell., verschwomm. Sehen, Hypertonie, Dyspepsie, Hautreakt. (Akne, Dermatitis), Muskelspasmen, periph. Ödem, Gesichtsöd., Gewichtszunahme; NW system. Glucocorticoide z. B. erhöhter Blutdruck, erhöhtes Infektionsrisiko, verzög. Wundheil., verring. Glukosetoler., Natriumretent. m. Ödembild., Muskelschwäche, Osteoporose, Glaukom, psych. Erkrank., pept. Ulzera, erhöhtes Thromboserisiko. Warnhinw.: Enth. Saccharose. Angaben gekürzt – weitere Einzelheiten entnehmen Sie bitte d. Fach- bzw. Gebrauchsinformation. Verschreibungspflichtig. Zulassungsinhaber: STADA Arzneimittel AG, Stadastraße 2–18, 61118 Bad Vilbel Örtlicher Vertreter: STADAPHARM GmbH, Stadastraße 2–18, 61118 Bad Vilbel Stand: Juli 2024
|
|
|
|
|
© STADA Arzneimittel AG, Stadastraße 2-18, 61118 Bad Vilbel, Tel.: +49 (0) 6101 603-0, Fax: +49 (0) 06101 603-259, www.stada.de, E-Mail: [email protected]
Vorstand: Peter Goldschmidt (Vorsitzender), Mark Keatley, Miguel Pagan Fernandez
Aufsichtsrat: Dr. Günter von Au (Vorsitzender)
Sitz der Gesellschaft: Bad Vilbel, Registergericht: Amtsgericht Frankfurt am Main HR B 71290
Diese E-Mail enthält vertrauliche und/oder rechtlich geschützte Informationen. Sollten Sie nicht der richtige Adressat sein oder diese E-Mail irrtümlich erhalten haben, informieren Sie bitte sofort den Absender und löschen anschließend diese E-Mail. Das unerlaubte Kopieren sowie die unbefugte Weitergabe des Inhalts dieser E-Mail sind nicht gestattet.
Die datenschutzrechtlichen Informationspflichten nach Art. 13 DS-GVO können Sie hier abrufen.
Bitte antworten Sie nicht auf diese E-Mail.
|
|
|
|
|
|
„Kompakt Nephrologie“ ist ein Titel der Biermann Verlag GmbH in Köln. Sie erhalten diese E-Mail, da Sie für diesen Newsletter angemeldet sind. Sie können in unserem Fachportal weitere Newsletter zu verschiedenen medizinischen Fachrichtungen abonnieren. Sollten Sie kein Interesse mehr an diesem Newsletter haben, können Sie sich hier abmelden. Haben Sie Fragen oder Anregungen zu unseren Themen und Inhalten, freuen wir uns auf Ihre E-Mail: [email protected].
Bitte beachten Sie, dass dieser Newsletter nur Angehörigen der Heilberufe gemäß HWG §10 zugänglich gemacht werden darf; das gilt auch für das Weiterempfehlen und Weiterleiten. Impressum: Biermann Verlag GmbH | MedCon Health Contents GmbH | HRB Bonn 11110 | HRB Köln 78926
Geschäftsführer: Dr. med. Hans Biermann
Hier vollständiges Impressum aufrufen
|
|
|
|
|