|
Liebe Leserinnen und Leser,
in der modernen Onkologie ist der „Status“ mehr als ein Detail – er ist Entscheidungsgrundlage, Selektionskriterium und Studiendesign zugleich.1 Ob BRCA, HRD oder Residualtumor: Beim fortgeschrittenen Ovarialkarzinom (FIGO III/IV) strukturieren diese Parameter die Therapielandschaft.1 Jede Patientin bringt andere Voraussetzungen mit und benötigt trotzdem eine auf sie angepasste Therapie.
Als Erstlinien-Erhaltungstherapie überzeugt der PARP-Inhibitor Rucaparib (Rubraca®) durch Wirksamkeit in sämtlichen Subgruppen – unabhängig von genetischem oder chirurgischem Status.2-5 Mit einem handhabbaren Sicherheitsprofil, stufenweiser Dosisanpassung und Langzeitdaten ermöglicht Rucaparib eine individualisierte Erhaltungstherapie.2-5 Zugelassen als Monotherapie in der Erstliniea und in der S3-Leitlinieb etabliert.1,2
Neuer Data-Cutoff – über die erste Progression hinaus
Die ATHENA-MONO-Studie erweitert den Zeithorizont: Der jüngst publizierte Data-Cutoff von Dr. Sharad Ghamande et al. analysiert zentrale Parameter wie die Zeit bis zur zweiten Progression (PFS2), bis zum Start der zweiten Therapielinie (erste Folgetherapie, TFST) und bis zum Start der dritten Therapielinie (zweite Folgetherapie, TSST).³ Das Ergebnis: Rucaparib demonstriert nicht nur initiale Wirksamkeit, sondern auch therapeutische Ausdauer.

PFS-Vorteil nach 4 Jahren – Langzeitwirksamkeit
Die von Kristeleit et al. präsentierten Langzeitdaten der ATHENA-MONO-Studie umfassen einen Beobachtungszeitraum von 4 Jahren für Rucaparib und 3,5 Jahren für Placebo – begleitet von einer engmaschigen Verlaufskontrolle durch Prüfärzte.4 Das Ergebnis: Rubraca® verlängert als Erstlinien-Erhaltungstherapie das prüfärztlich bewertete mediane PFS signifikant – in sämtlichen Subgruppen, unabhängig von BRCA- oder HRD-Status.4,5

Sicherheitsprofil in der Hand
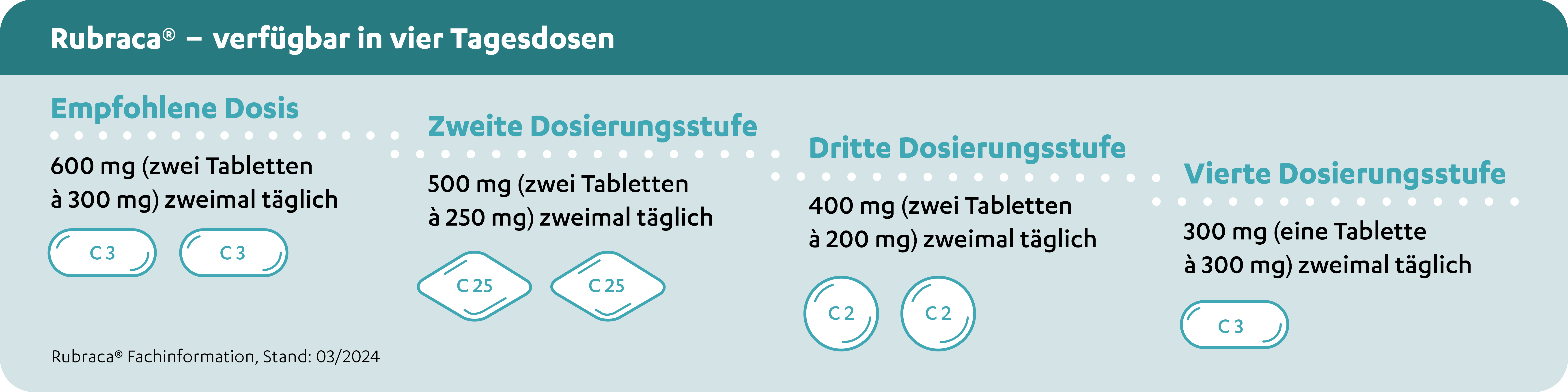
Die Erhaltungstherapie mit Rucaparib wird mit einer einheitlichen Anfangsdosis von 1200 mg eingeleitet – ohne Kalkulationen auf Basis von Körpergewicht und Thrombozytenzahl – bietet jedoch im Verlauf der Therapie eine individualisierbare Flexibilität dank vier möglicher Tagesdosen (600 mg, 800 mg, 1000 mg, 1200 mg).2,6 Mit einer medianen Dosisintensität von
89 %, die über den gesamten Behandlungszeitraum aufrechterhalten werden konnte, demonstrierte Rucaparib ein handhabbares Sicherheitsprofil.2,6
a Rucaparib ist zugelassen als Monotherapie zur Erhaltungstherapie bei Patientinnen mit fortgeschrittenem (FIGO-Stadien III und IV) high-grade epithelialen Ovarial-, Eileiter- oder primärem Peritonealkarzinom, die nach Abschluss einer platinbasierten Erstlinien-Chemotherapie in Remission sind (vollständig oder partiell).
b S3-Leitlinie „Diagnostik, Therapie und Nachsorge maligner Ovarialtumoren“ vom Leitlinienprogramm Onkologie unter Federführung der Deutschen Gesellschaft für Gynäkologie und Geburtshilfe e.V. (DGGG) und unter Mitwirkung von 30 Fachgesellschaften und Organisationen.
Abkürzungen
BRCAmut = Mutation in BRCA1 oder BRCA2
HRD = homologe Rekombinationsdefizienz
ITT = Intention-to-Treat
mPFS = medianes progressionsfreies Überleben
PARPi = Poly(ADP-Ribose)-Polymerase-Inhibitor
Referenzen
- Leitlinienprogramm Onkologie. S3-Leitlinie maligne Ovarialtumoren, v. 6.0, 2024, AWMF-Nr: 032-035OL.
- Rubraca® Fachinformation, Stand 03/2024.
- Ghamande S et al. Int J Gynecol Cancer. 2025;35(2):100319.
- Kristeleit R et al. Abstract 49MO. Ann Oncol. 2024;9(suppl_5):1-19.
- Monk BJ et al. J Clin Oncol. 2022;40(34):3952-3964.
- O’Malley D et al. Abstract 5554. J Clin Oncol. 2024;42 suppl_16.
Pflichttext
RUBRACA® 200 mg / 250 mg / 300 mg Filmtabletten. Wirkstoff: Rucaparib. Wirkstoff: Rucaparib. Zusammensetzung: Jede Tablette enthält Rucaparib-(+)-camsilat, entsprechend 200 mg / 250 mg / 300 mg Rucaparib. Sonstige Bestandteile: Tablettenkern: Mikrokristalline Cellulose, Carboxymethylstärke-Natrium (Typ A), Hochdisperses Siliciumdioxid, Magnesiumstearat; Tablettenüberzug: Poly(vinylalkohol) (E1203), Titandioxid (E171), Macrogol 4000 (E1521), Talkum (E553b), Rubraca 200 mg: Brillantblau FCFAluminiumsalz (E133), Indigocarmin-Aluminiumsalz (E132); Rubraca 300 mg: Eisen(III)-hydroxid-oxid x H2O (E172). Anwendungsgebiete: Rubraca wird angewendet als Monotherapie für die Erhaltungstherapie bei erwachsenen Patientinnen mit fortgeschrittenem (FIGO-Stadien III und IV) high-grade epithelialem Ovarial-, Eileiter- oder primärem Peritonealkarzinom, die nach Abschluss einer platinbasierten Erstlinien-Chemotherapie in Remission sind (vollständig oder partiell). Rubraca ist indiziert als Monotherapie für die Erhaltungstherapie bei erwachsenen Patientinnen mit platinsensitivem, rezidiviertem, high-grade epithelialem Ovarial, Eileiter- oder primärem Peritonealkarzinom, die nach platinbasierter Chemotherapie in Remission sind (vollständig oder partiell). Gegenanzeigen: Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile. Stillen. Nebenwirkungen: Sehr häufig: Anämie, Thrombozytopenie, Neutropenie, Leukopenie, verminderter Appetit, erhöhtes Kreatinin im Blut, Hypercholesterinämie, Dysgeusie, Schwindel, Dyspnoe, Übelkeit, Erbrechen, Diarrhoe, Dyspepsie, Schmerzen des Abdomens, erhöhte Alanin-Aminotransferase, erhöhte Aspartat-Aminotransferase, Lichtempfindlichkeitsreaktion, Ausschlag, Müdigkeit, Fieber. Häufig: Myelodysplastisches Syndrom / akute myeloische Leukämie, Lymphopenie, febrile Neutropenie, Überempfindlichkeitsreaktionen, Dehydration, intestinale Obstruktion, Stomatitis, erhöhte Transaminasen, makulopapulöser Ausschlag, palmar-plantares Erythrodysästhesiesyndrom, Erythem. Abgabestatus: Verschreibungspflichtig. Weitere Angaben: siehe Fachinformation. Inhaber der Zulassung: pharmaand GmbH, Taborstrasse 1, 1020 Wien, Österreich. Örtlicher Vertreter: pharmaand Deutschland GmbH, c/o ABC Workspaces Bertha-Benz-Straße 5, D-10557 Berlin, Deutschland. E-Mail: [email protected]. Servicehotline für Produktanfragen: Tel: +49 (0)8005892665. Stand der Information: März 2024.
|