|
|
Liebe Leserinnen und Leser,
das entzündlich* Trockene Auge benötigt aufgrund seiner Chronizität eine langfristige Behandlung.1 Bei kontinuierlicher Anwendung sorgt Ikervis® für eine signifikante Verbesserung der Augenoberfläche und eine anhaltende Symptomlinderung1-5 – mit nur einem Tropfen täglich2,3,6,7. Dies konnte in der europaweit angelegten Studie PERSPECTIVE auch für die Langzeitanwendung über 12 Monate bestätigt werden.1
In dieser prospektiven, multizentrischen Studie wurden die Wirksamkeit, Sicherheit und Verträglichkeit von Ciclosporin A in einer unkonservierten kationischen Emulsion bei der Behandlung des Trockenen Auges unter realen klinischen Bedingungen untersucht. Mit Hilfe des CFS-Grades (Corneal Fluorescein Staining) wurden die Schäden der Hornhautoberfläche objektiv erfasst.
Bereits ab Woche 4 trat eine signifikante Verbesserung der Zeichen und Symptome des Trockenen Auges auf, dies hielt über den gesamten
Studienzeitraum von 12 Monaten an.
|
|
|
|
|
Abb. 1.: Reduktion des CFS-Grades (Real World Studie PERSPECTIVE; n=472), visuelle Darstellung.1 Der mittlere CFS-Score sank signifikant von 2,56 auf 1,10 in Monat 12 (p<0,0001;
Abb. 1). Ebenso verbesserte sich im selben Zeitraum die Schwere des Augenlids- und Bindehauterythems signifikant. Dabei war Ciclosporin in kationischer Emulsion im Allgemeinen gut verträglich. Die beobachteten Nebenwirkungen waren überwiegend mild oder moderat und vorübergehend. Als häufigste behandlungsbezogene Nebenwirkungen wurden Irritationen (29,7 %) oder Schmerzen (13,9 %) genannt.1
|
Ciclosporin in unkonservierter kationischer Emulsion Das Besondere an Ikervis® ist die Formulierung als unkonservierte kationische Emulsion.7 Kationische Emulsionen imitieren funktionell einen gesunden Tränenfilm und sind effektive Trägersysteme für lipophile Wirkstoffe.7-10 |
|
|
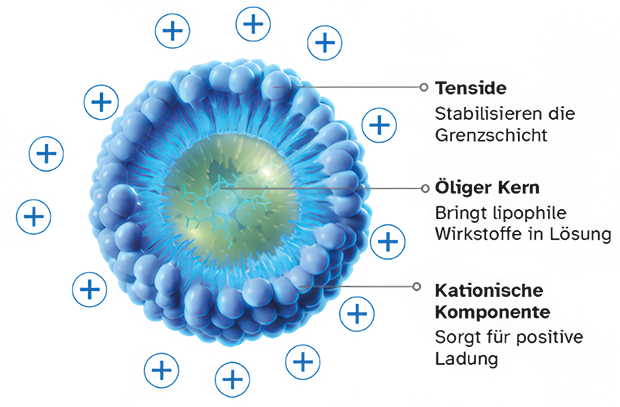 |
Abb. 2: Nanotropfen einer kationischen Emulsion, adaptiert nach Daull P, et al. J Pharm Pharmacol 2014;66:531–413.10 Emulgiert in der wässrigen Phase enthalten kationische Emulsionen positiv geladene Nanotropfen mit einem öligen Kern, der sehr gut zum Lösen lipophiler Wirkstoffe wie z. B. Ciclosporin A geeignet ist (Abb. 2).8,10 Elektrostatische Wechselwirkungen sorgen für eine verbesserte Verteilung der Tropfen im Tränenfilm. Sie werden von der negativ geladenen Muzinschicht des Tränenfilms und den negativ geladenen Epithelzellen angezogen.10 Dies sorgt für eine gute Verteilung und längere Verweildauer der Nanotropfen auf der Augenoberfläche.10
Sie möchten mehr über die Wirksamkeit von Ikervis® und der Besonderheit der kationischen Emulsion erfahren? Besuchen Sie unser SEE-Portal. |
 |
Herzliche Grüße aus München Ihr Team der Santen GmbH |
|
|
CFS, Corneal Fluorescein Staining (Hornhautfärbung mit Fluoreszein) * Ikervis® ist indiziert zur Behandlung schwerer Keratitis bei Erwachsenen mit Trockenen Augen, bei denen trotz Behandlung mit Tränenersatzmitteln keine Besserung eingetreten ist.3 Referenzen: 1. Geerling G, et al. Ophthalmol Ther 2022;11:1101−17.
2. Pisella PJ, et al. Clin Ophthalmol 2018;12:289−99.
3. Ikervis® (Ciclosporin). Fachinformation. Santen. Letzte Aktualisierung Januar 2022.
4. Labetoulle M, et al. Clin Ther 2018;40:1894−906.
5. Messmer EM, et al. Eur J Ophthalmol 2023;33:1294−307.
6. Leonardi A, et al. Eur J Ophthalmol 2016;26:287−96.
7. Hoy SM. Drugs 2017;77:1909−16.
8. Daull P, et al. Glauc Open Access 2017; 2: 107.
9. Daull P, et al. J Ocul Pharmacol Th 2020;36:355–365.
10. Daull P, et al. J Pharm Pharmacol 2014;66:531–413.
|
IKERVIS® 1 mg/ml Augentropfen, Emulsion. Wirkstoff: Ciclosporin. Qualitative und quantitative Zusammensetzung: Ein ml Emulsion enthält 1 mg Ciclosporin. Sonstiger Bestandteil mit bekannter Wirkung: Ein ml Emulsion enthält 0,05 mg Cetalkoniumchlorid. Sonstige Bestandteile: Mittelkettige Triglyceride, Cetalkoniumchlorid, Glycerol, Tyloxapol, Poloxamer 188, Natriumhydroxid (zur Einstellung des pH-Werts), Wasser für Injektionszwecke. Anwendungsgebiete: Behandlung schwerer Keratitis bei Erwachsenen mit trockenen Augen, bei denen trotz Behandlung mit Tränenersatzmitteln keine Besserung eingetreten ist. Gegenanzeigen: Überempfindlichkeit gegen Ciclosporin oder einen der sonstigen Bestandteile. Okulare oder periokulare Malignitäten oder prämaligne Krankheitsbilder. Akute oder vermutete okulare oder periokulare Infektion. Nebenwirkungen: Sehr häufig: Augenschmerzen, Augenreizung. Häufig: Erythem des Augenlids, Verstärkte Produktion von Tränenflüssigkeit, Okulare Hyperämie, Verschwommenes Sehen, Augenlidödem, Konjunktivale Hyperämie, Pruritus am Auge. Gelegentlich: Bakterielle Keratitis, Herpes zoster am Auge; Bindehautödem, Tränenbildungsstörung, Augensekret, Bindehautreizung, Konjunktivitis, Fremdkörpergefühl in den Augen, Ablagerungen am Auge, Keratitis, Blepharitis, Chalazion, Hornhautinfiltrate, Hornhautnarbe, Pruritus am Augenlid, Iridocyclitis, Augenbeschwerden; Reaktion an der Verabreichungsstelle; Kopfschmerz. Verschreibungspflichtig. Inhaber der Zulassung: Santen Oy, Niittyhaankatu 20, 33720 Tampere, Finnland. Örtlicher Vertreter: Santen GmbH, 80636 München. Stand der Information: 01/2022. Weitere Informationen sind der veröffentlichten Fachinformation zu entnehmen. REF-9860 01/2022
Santen GmbH • Erika-Mann-Straße 21 • 80636 München • [email protected] Geschäftsführer: Patrick Süther, Sitz: München, Registergericht München HRB 107 705, UST-IdNr. DE 164493885 |
|
|
IKERVI-DE-250010 SAN 03.2025
|
|
|
|
|
|
„Ophthalmologische Nachrichten“ ist ein Titel der Biermann Verlag GmbH in Köln. Sie erhalten diese E-Mail, da Sie für diesen Newsletter angemeldet sind. Sie können in unserem Fachportal weitere Newsletter zu verschiedenen medizinischen Fachrichtungen abonnieren. Sollten Sie kein Interesse mehr an diesem Newsletter haben, können Sie sich hier abmelden. Haben Sie Fragen oder Anregungen zu unseren Themen und Inhalten, freuen wir uns auf Ihre E-Mail: [email protected]. Bitte beachten Sie, dass dieser Newsletter nur Angehörigen der Heilberufe gemäß HWG §10 zugänglich gemacht werden darf; das gilt auch für das Weiterempfehlen und Weiterleiten.
Impressum: Biermann Verlag GmbH | MedCon Health Contents GmbH | HRB Bonn 11110 | HRB Köln 78926
Geschäftsführer: Dr. med. Hans Biermann
Hier vollständiges Impressum aufrufen
|
|
|
|
|
|