Axiale Spondyloarthritis
Geringe Uveitis-Inzidenz unter dualer Hemmung von IL-17A und IL-17F
Sehr geehrte Leser:innen,
Extraartikuläre Manifestationen, wie die akute anteriore Uveitis (AAU),
treten bei Spondyloarthritiden häufig auf, insbesondere bei
Patient:innen mit Human-Leukocyte-Antigen (HLA)-B27-positiver axialer
Spondyloarthritis (axSpA).1 Gemäß der ASAS (Assessment of SpondyloArthritis international
Society)-EULAR (European Alliance of Associations for
Rheumatology)-Leitlinie der rheumatologischen Fachgesellschaften wird empfohlen Patient:innen mit rezidivierender AAU mit monoklonalen Tumornekrosefaktor-Inhibitoren (TNFi) zu behandeln.2
Neben TNFi gewinnen auch andere Therapien an Bedeutung. Ein Beispiel
dafür ist der duale Interleukin-17A- und -17F-Inhibitor Bimekizumab▼
(BKZ).2
Ein spannendes Video mit Prof. Dr. Martin Rudwaleit, Direktor der
Universitätsklink für Innere Medizin und Rheumatologie, Klinikum
Bielefeld Rosenhöhe, präsentiert aktuelle gepoolte Daten aus den
Phase-III-Studien BE MOBILE 1 und 2 zur axSpA.*,3,4
Die Ergebnisse deuten
darauf hin, dass Patient:innen unter der Behandlung mit BKZ eine
niedrigere AAU-Inzidenz aufweisen im Vergleich zur Placebo-Gruppe.**,4
|
|
|
In dieser aktuellen Post-hoc-Analyse wurden die Uveitis-Inzidenzen
untersucht.3 Ergebnisse der Phase-III-Studien zeigen: In der
BE-MOBILE-1-Studie hatten 1,6 % (n=2/128) der mit BKZ-Behandelten ein
Uveitis-Ereignis, verglichen mit 4,8 % (n=6/126) unter Placebo
(pnominal=0,145). In der BE-MOBILE-2-Studie hatten keine mit BKZ
behandelten Patient:innen (n=0/221) ein Uveitis-Ereignis, im Vergleich
zur Placebo-Gruppe, in der 4,5 % (n=5/111) ein Uveitis-Ereignis hatten
(pnominal=0,002).3
Fälle einer Uveitis wurden außerdem als Inzidenz und als
expositionsbereinigte Inzidenzraten (EAIR) pro 100 Patientenjahre (PJ)
angegeben. Der Vergleich der Uveitis-Inzidenz während der doppelblinden
Phase (Woche 0–16) der beiden Phase-III-Studien ergab: In der auf
Placebo randomisierten Gruppe war Uveitis bei 4,6 % (n=11/237, EAIR
15,4/100 PJ, 95 %-Konfidenzintervall [KI] 7,7; 27,5; pnominal=0,001)
aufgetreten, während unter BKZ 0,6 % (n=2/349) betroffen waren (EAIR
1,8/100 PJ, 95 %- KI 0,2; 6,7; Abb. 1).3 Die Uveitis führte bei zwei
Studienteilnehmer:innen im Placebo-Arm zum Behandlungsabbruch.3
|
|
|
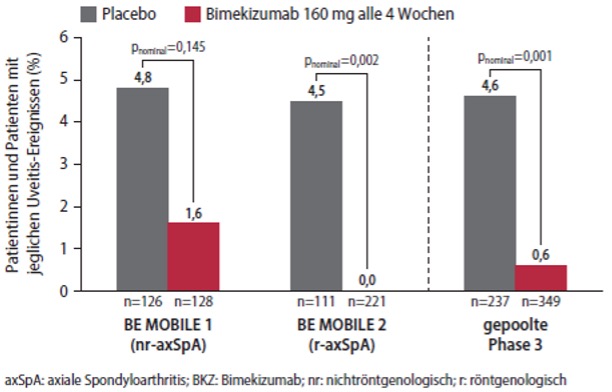
Abbildung 1: Uveitis-Inzidenzen in der doppelblinden Behandlungsphase
(Wochen 0−16) von BE MOBILE 1 und BE MOBILE 2 (BKZ vs. Placebo*).
Modifiziert nach 4.
|
*Beide axSpA-Studien zu BKZ (160 mg subkutan alle 4 Wochen) zeigten bis
zu Woche 16 eine im Vergleich zu Placebo statistisch signifikante und
klinisch bedeutsame Verbesserung der Anzeichen und Symptome der axSpA,
definiert durch den primären Endpunkt ASAS40 (40 %ige Verbesserung gemäß
den Kriterien der ASAS).3
**Bimekizumab ist nicht zur Behandlung von Uveitis zugelassen.
Bimekizumab ist zugelassen zur Behandlung Erwachsener mit mittelschwerer
bis schwerer Plaque-Psoriasis, aktiver Psoriasis-Arthritis, aktiver
axSpA und aktiver mittelschwerer bis schwerer Hidradenitis suppurativa.5
▼ Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse
über die Sicherheit. Bitte melden Sie jeden Verdachtsfall einer Nebenwirkung über das Bundesinstitut für Impfstoffe und
biomedizinische Arzneimittel: www.pei.de
|
|
Pflichttext | DE-BK-2400961
|
|
Literatur
|
|
1.
|
Rademacher J et al., Ther Adv Musculoskelet Dis 2020, 12:1759720X20951733
|
|
2.
|
Ramiro S et al., Ann Rheum Dis 2023, 82:19–34
|
|
3.
|
van der Heijde D et al., Ann Rheum Dis 2023, 82:515–526
|
|
4.
|
Brown MA et al., Ann Rheum Dis 2024, 0:1–9
|
|
5.
|
Fachinformation Bimzelx®, Stand August 2024
|
|
|
|
|
|
„Orthopädische • Unfallchirurgische Nachrichten“ ist ein Titel der Biermann Verlag GmbH in Köln. Sie erhalten diese E-Mail, da Sie für diesen Newsletter angemeldet sind. Sie können in unserem Fachportal weitere Newsletter zu verschiedenen medizinischen Fachrichtungen abonnieren. Sollten Sie kein Interesse mehr an diesem Newsletter haben, können Sie sich hier abmelden. Haben Sie Fragen oder Anregungen zu unseren Themen und Inhalten, freuen wir uns auf Ihre E-Mail: [email protected]. Bitte beachten Sie, dass dieser Newsletter nur Angehörigen der Heilberufe gemäß HWG §10 zugänglich gemacht werden darf; das gilt auch für das Weiterempfehlen und Weiterleiten.
Impressum: Biermann Verlag GmbH | MedCon Health Contents GmbH | HRB Bonn 11110 | HRB Köln 78926
Geschäftsführer: Dr. med. Hans Biermann
Hier vollständiges Impressum aufrufen
|
|
|
|
|
|