Colitis ulcerosa: Ist Disease Clearance ein realistisches Therapieziel

|
| |
|
Liebe Leserinnen und Leser,
|
| |
|
die Therapieziele bei Colitis ulcerosa (CU) haben sich in den letzten Jahren weiterentwickelt: Inzwischen wird die „Disease Clearance“a,b – der zusammengesetzte Endpunkt aus klinischer, endoskopischer und histologischer Remission (minimale histologische Krankheitsaktivität) – als neues zukünftiges Therapieziel bei CU-Patient:innen diskutiert.1 Doch warum sollte eine Disease Clearance angestrebt werden? Und ist die Disease Clearance bei CU wirklich ein realistisches Therapieziel?
|
| |
|
Disease Clearance bei Colitis ulcerosa
|
| |
|
Die Disease Clearancea,b kann als fehlender Nachweis einer Krankheitsaktivität bei CU gesehen werden. Studiendaten weisen darauf hin, dass CU-Patient:innen mit einer endoskopischen plus einer histologischen Remission ein deutlich niedrigeres Rezidivrisiko aufwiesen als die Patient:innen, die nur eine klinische Remission erzielt hatten.2 Das macht das Erreichen einer Disease Clearance zu einem erstrebenswerten Therapieziel für Ihre CU-Patient:innen – aber ist es auch realistisch?
|
| |
|
Mit Entyvio® sowohl kurz- als auch langfristige Therapieziele erreichen
|
| |
|
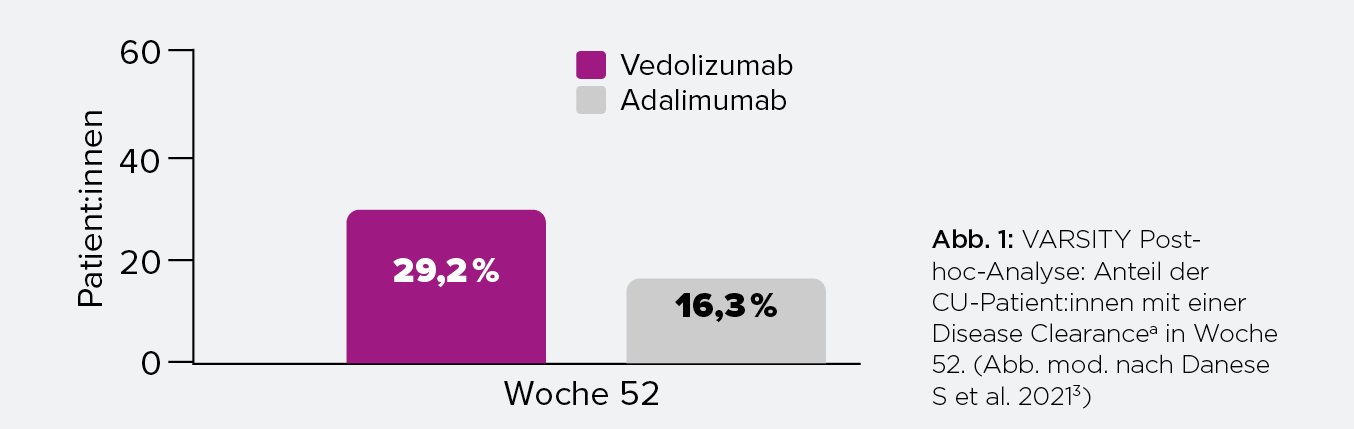
Eine Post-hoc-Analyse der VARSITY-Studie lieferte Hinweise darauf, dass unter dem α4β7-Integrin-Antagonisten Vedolizumab (Entyvio®c) fast 30 % der CU-Patient:innen nach einem Jahr den zusammengesetzten Endpunkt Disease Clearancea erreichen können (Abb. 1).3
|
| |
|
| |
|
In der VERDICT-Studied, die das optimale Therapieziel bei Patient:innen mit mittelschwerer bis schwerer CU untersucht, erreichten in der Interimsanalyse 55,2 % der Biologika-naiven CU-Patient:innen (n = 183) nach 32 Wochen Behandlung mit Entyvio® den zusammengesetzten Endpunkt einer steroidfreien Disease Clearance.b,4
|
| |
|
Kurze Frage – kurze Antwort
|
| |
Ist Disease Clearance bei CU als Therapieziel realistisch?
Prof. Dr. med. Timo Rath, Erlangen, stellt in einem 3-Minuten-Video kurz und kompakt das Konzept der Disease Clearance und aktuelle Studienergebnisse dazu vor. Schauen Sie einfach mal rein!
|
| |

|
| |
|
Wir freuen uns über Ihr Interesse!
|
| |
Herzliche Grüße
Ihr CED Team der Takeda Pharma Vertrieb GmbH & Co. KG
|
| |

|
| |
|
| |
|
a Disease Clearance (VARSITY Post-hoc): zusammengesetzter Endpunkt aus 1. Klinische Remission: partieller Mayo-Score ≤ 2 und kein individueller Subscore > 1 (exklusive Sigmoidoskopie-Subscore); 2. Endoskopische Verbesserung: endoskopischer Subscore ≤ 1; 3. Minimale histologische Krankheitsaktivität: Robarts Histology Index (RHI) < 5.3
|
| |
|
b Disease Clearance (VERDICT): zusammengesetzter Endpunkt aus 1. Steroidfreie symptomatische Remission: Mayo-Subscore für rektale Blutungen = 0; 2. Endoskopische Remission: endoskopischer Mayo-Score ≤ 1; 3. Histologische Remission: Geboes-Score < 2B.0.4
|
| |
|
c Vedolizumab ist zugelassen für die Behandlung von erwachsenen Patient:innen mit mittelschweren bis schweren aktiven Formen von Colitis ulcerosa/Morbus Crohn, die entweder auf konventionelle Therapie oder einen der Tumornekrosefaktor-alpha (TNFα)-Antagonisten unzureichend angesprochen haben, nicht mehr darauf ansprechen oder eine Unverträglichkeit gegen eine entsprechende Behandlung aufweisen.6,7
|
| |
|
d VERDICT: actiVE ulcerative colitis, a RanDomIsed Controlled Trial. Limitation der VERDICT-Studie: Abweichend zur zugelassenen Indikation von Entyvio® wurden auch Patient:innen mit milder Krankheitsaktivität in die Studie eingeschlossen (Behandlungsgruppe 3 [n = 213]: 4,7 % [n = 10] der Patient:innen).5
|
| |
|
Literatur
|
- Colombel JF. Gastroenterol Hepatol (N Y) 2021; 17(5): 233-235
- Yoon H et al. Gastroenterology 2020; 159: 1262-1275.e7
- Danese S et al. J Crohns Colitis 2021; 15(S1): S305
- Jairath V et al. UEGW 2024, poster presentation PP0556
- Jairath V et al. BMJ Open Gastroenterol 2024; 11(1): e001218
- Fachinformation Entyvio® 300 mg Pulver für ein Konzentrat zur Herstellung einer Infusionslösung, aktueller Stand
- Fachinformation Entyvio® 108 mg Injektionslösung in einer Fertigspritze/Entyvio® 108 mg Injektionslösung in einem Fertigpen, aktueller Stand
|
| |

|
| |
Entyvio® 300 mg, Pulver für ein Konzentrat zur Herstellung einer Infusionslösung, Entyvio® 108 mg Injektionslösung in einer Fertigspritze; Entyvio® 108 mg Injektionslösung in einem Fertigpen
Wirkstoff: Vedolizumab
|
| |
|
Zusammensetzung: Entyvio 300 mg, Pulver: Jede Durchstechflasche enthält 300 mg Vedolizumab; nach Rekonstitution enthält 1 ml Infusionslösung 60 mg Vedolizumab. Sonstige Bestandteile: L-Histidin, L-Histidin-Monohydrochlorid, L-Arginin-Hydrochlorid, Saccharose, Polysorbat 80. Entyvio 108 mg Injektionslösung (subkutan): Jede Fertigspritze/jeder Fertigpen enthält 108 mg Vedolizumab in 0,68 ml. Sonstige Bestandteile: Citronensäure-Monohydrat, Natriumcitrat-Dihydrat, L-Histidin, L-Histidin-Monohydrochlorid, L-Arginin-Hydrochlorid, Polysorbat 80, Wasser für Injektionszwecke. Anwendungsgebiete: Colitis ulcerosa: Behandlung von erwachsenen Patienten mit mittelschwerer bis schwerer aktiver Colitis ulcerosa, die entweder auf konventionelle Therapie oder einen der Tumornekrosefaktor-alpha (TNFα)-Antagonisten unzureichend angesprochen haben, nicht mehr darauf ansprechen oder eine Unverträglichkeit gegen eine entsprechende Behandlung aufweisen. Morbus Crohn: Behandlung von erwachsenen Patienten mit mittelschwerem bis schwerem aktiven Morbus Crohn, die entweder auf konventionelle Therapie oder einen der Tumornekrosefaktor-alpha (TNFα)-Antagonisten unzureichend angesprochen haben, nicht mehr darauf ansprechen oder eine Unverträglichkeit gegen eine entsprechende Behandlung aufweisen. Pouchitis (nur Entyvio 300 mg Pulver für ein Konzentrat zur Herstellung einer Infusionslösung): Behandlung von erwachsenen Patienten mit mittelschwerer bis schwerer aktiver chronischer Pouchitis, die sich wegen Colitis ulcerosa einer Proktokolektomie, bei der ein ileoanaler Pouch angelegt wurde, unterzogen haben, und auf eine Antibiotikabehandlung nur unzureichend oder gar nicht angesprochen haben. Gegenanzeigen: Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile. Aktive schwere Infektionen wie Tuberkulose, Sepsis, Cytomegalievirus, Listeriose und opportunistische Infektionen, wie z.B. progressive multifokale Leukoenzephalopathie (PML). Nebenwirkungen: Sehr häufig: Nasopharyngitis, Kopfschmerzen, Arthralgie; Häufig: Pneumonie, Clostridium-difficile-Infektion, Bronchitis, Gastroenteritis, Infektion der oberen Atemwege, Grippe, Sinusitis, Pharyngitis, Herpes Zoster, Parästhesie, Hypertonie, Schmerzen im Oropharynx, Nasenverstopfung, Husten, Analabszess, Analfissur, Übelkeit, Dyspepsie, Obstipation, Bauch aufgetrieben, Flatulenz, Hämorrhoiden, Rektalblutung*, Ausschlag, Pruritus, Ekzem, Erythem, Nächtliche Schweißausbrüche, Akne, Muskelspasmen, Rückenschmerzen, Muskuläre Schwäche, Ermüdung, Schmerzen in den Extremitäten, Fieber, Reaktionen im Zusammenhang mit einer Infusion (Asthenie* und Brustkorbbeschwerden*); Reaktion an der Injektionsstelle (einschließlich: Schmerzen an der Infusionsstelle und Irritation an der Infusionsstelle); Gelegentlich: Atemwegsinfektion, vulvovaginale Candidose, orale Candidose, verschwommenes Sehen, Follikulitis, Schüttelfrost, Kältegefühl; Sehr selten: anaphylaktische Reaktion, anaphylaktischer Schock. Nicht bekannt: Interstitielle Lungenerkrankung. *Berichtet bei Pouchitis Verschreibungspflichtig. EU-Zulassungsinhaber: Takeda Pharma A/S, Dänemark Stand der Information: Juli 2023
|
| |
|
|
„Kompakt Gastroenterologie“ ist ein Titel der Biermann Verlag GmbH in Köln. Sie erhalten diese E-Mail, da Sie für diesen Newsletter angemeldet sind. Sie können in unserem Fachportal weitere Newsletter zu verschiedenen medizinischen Fachrichtungen abonnieren. Sollten Sie kein Interesse mehr an diesem Newsletter haben, können Sie sich hier abmelden. Haben Sie Fragen oder Anregungen zu unseren Themen und Inhalten, freuen wir uns auf Ihre E-Mail: [email protected]. Bitte beachten Sie, dass dieser Newsletter nur Angehörigen der Heilberufe gemäß HWG §10 zugänglich gemacht werden darf; das gilt auch für das Weiterempfehlen und Weiterleiten.
Impressum: Biermann Verlag GmbH | MedCon Health Contents GmbH | HRB Bonn 11110 | HRB Köln 78926
Geschäftsführer: Dr. med. Hans Biermann
Hier vollständiges Impressum aufrufen
|
|
|
|
|
|