|
Symposium auf dem DGHNO 2025
Dupilumab bei CRSwNP: Remission ist möglich
Zur Behandlung der chronischen Rhinosinusitis mit Nasenpolypen (CRSwNP) steht seit 2019 das Biologikum Dupilumab (Dupixent®)* zur Verfügung. Ein Symposium im Rahmen des DGHNO 2025 in Frankfurt ging jetzt der Frage nach, welche neuen Therapieziele gesteckt werden können und inwieweit eine Remission der Erkrankung unter Therapie realistisch erscheint.
„Remission bedeutet im Fall der CRSwNP: Anhaltende Symptomkontrolle für ≥ 12 Monate in Verbindung mit dem Fehlen von Anzeichen einer aktiven Erkrankung, die durch die Nasenendoskopie beurteilt wird“, so PD Dr. Sven Becker, Tübingen. Er betonte die Bedeutung der subjektiven Verbesserung für die Patient*innen: „Wichtig ist die von Patient*innen angegebene Kontrolle – die Verbesserungen ersichtlich im SNOT-22 und in der Visual Analogskala (VAS).“ Er präsentierte dazu aktuelle Daten aus dem PolyREG-Register. Nach einem Jahr erfüllten hier 63,9 % die Kriterien für eine Krankheitskontrolle; in Kombination mit einer Nasenendoskopie erreichten 45,7 % eine Remission [1]. Nach zweijähriger Behandlung erreichten 50,0 % der Patient*innen unter Dupilumab eine Krankheitskontrolle und 43,7 % befanden sich in Remission.
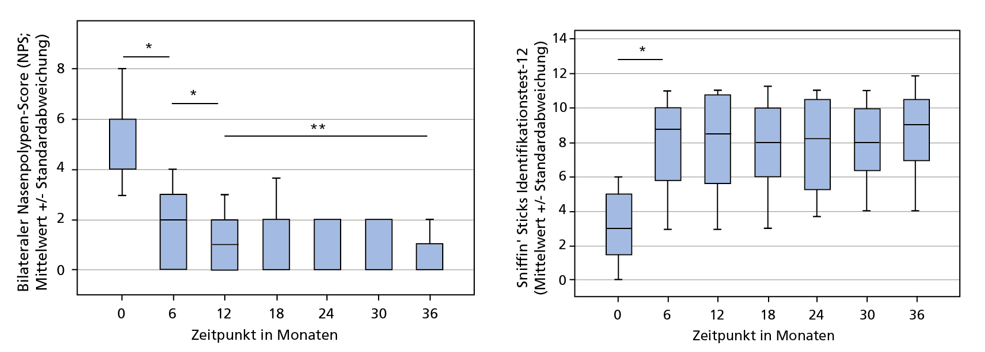
Abb. 1 Dupilumab reduzierte über 36 Monate signifikant den NPS-Score (links) und verbesserte das Riechvermögen (rechts), *p < 0.001; **p < 0.05 [mod. nach 2].
Verbesserung den Riechvermögens und Dupilumab
Auch in einer deutschen Real-World-Studie war die Krankheitslast unter Dupilumab bereits nach 6 Monaten signifikant gesunken mit anhaltenden Effekten über 36 Monate. Außerdem sank der NPS um durchschnittlich 5,3 Punkte und das Riechvermögen verbesserte sich (Abb. 1). 3 von 4 Patient*innen erreichten außerdem nach 36 Monaten eine Normosmie oder Hyposmie [2]. Auch in der italienischen DUPIREAL-Studie hatten sich der NPS um rund 5 Punkte und das Riechvermögen verbessert [3].
Dupilumab blockiert zielgerichtet die Signalweitergabe zweier Treiber der Typ-2-Inflammation, die der CRSwNP in bis zu 80 % der Fälle zugrunde liegt [4,5]. Die EU-Zulassung zur Behandlung der CRSwNP beruht auf den Ergebnissen der Phase-III-Studien SINUS-24 (24 Wochen) und SINUS-52 (52 Wochen). Diese hatten gezeigt, dass die Krankheitslast schnell abnimmt und Lebensqualität und Riechvermögen sich deutlich bessern [6,7].
Fazit
Die rasche und anhaltende Verbesserung der Beschwerden unter Dupilumab regte die Definition neuer Therapieziele an – so legen Real World-Daten eine gute Kontrolle bis hin zur Remission nahe. Erste Daten zeigen eine Remission unter Dupilumab bei gut der Hälfte der Patient*innen.
Operationen im Zusammenspiel mit Biologika – was wissen wir?
Prof. Martin Wagenmann, Düsseldorf, gab in seinem Vortrag einen kurzen Überblick über die Studienlage zu funktionellen endoskopischen Nasennebenhöhlenoperationen und Therapie mit Biologika im Vergleich und fokussierte sich dabei auf das Riechvermögen, das von Patient*innen als besonders wichtig eingestuft wird. Sein Fazit: „Wir sehen aktuell einen Paradigmenwechsel in der Therapie der CRSwNP. Uns stehen Biologika als Therapieoption bei Patient*innen mit schwerer chronischer Rhinosinusitis zur Verfügung und in den Real-World-Studien zeigt sich durch die Bank weg, dass im klinischen Alltag die Ergebnisse sogar eher noch besser sind als in den Phase-III-Studien. Wir können Revisionsoperationen offensichtlich durch die Anwendung von Biologika vermeiden.“
* Dupilumab ist zugelassen zur Behandlung von Erwachsenen mit schwerer CRSwNP, die mit systemischen Kortikosteroiden und / oder chirurgischem Eingriff nicht ausreichend kontrolliert werden kann [5].
Referenzen
[1] Otten JJ et al. Allergy 2025; 80: 1166–1168
[2] Huber P et al. Allergy 2024; 79: 3108–3117
[3] De Corso E et al. Allergy 2023; 78: 2669–2683
[4] Chaaban MR et al. Am J Rhinol Allergy 2013; 27(6): 473–478
[5] Fachinformation Dupixent® 300 mg, Stand November 2024
[6] Bachert C et al. Lancet 2019; 394: 1638–1650 inkl. Appendix
[7] Mullol J et al. J Allergy Clin Immunol Pract 2022; 10: 1086–1095
Pflichttext Dupilumab
Mit freundlicher Unterstützung von Sanofi und Regeneron
MAT-DE-2502512 -1.0-06/2025
Sanofi-Aventis Deutschland GmbH
sanofi.de
Herausgeber
Sanofi-Aventis Deutschland GmbH
Industriepark Höchst, K703, 65926 Frankfurt
Kontakt
E-Mail: [email protected]
|