|
Veränderung von Mucus Plugs bei Fasenra®-Patient:innen

|
|
Fasenra® ist angezeigt als Add-on-Erhaltungstherapie bei erwachsenen Patient:innen mit schwerem eosinophilem Asthma, das trotz hochdosierter inhalativer Corticosteroide plus lang wirksamer Beta-Agonisten unzureichend kontrolliert ist. Eine Erhaltungstherapie mit ICS/LABA als Hintergrundmedikation ist fortzusetzen.
Liebe Leser:innen,
die Phänotypisierung von schwerem Asthma wird immer wichtiger, vor allem wenn ein Biologikum zum Einsatz kommen soll.1 Gerade bei der Behandlung von schwerem eosinophilen Asthma (SEA) lohnt sich ein genauerer Blick auf die zugelassenen Therapieoptionen und deren Wirkmechanismen. Beispielsweise entfaltet der Anti-IL-5-Rezeptor-Antikörper Fasenra®* seine rasche Wirkung durch die nahezu vollständige Entfernung der Eosinophilen innerhalb von 24 Stunden.2
ERS 2024: Einfluss von Fasenra® auf die Atemwegspathologie
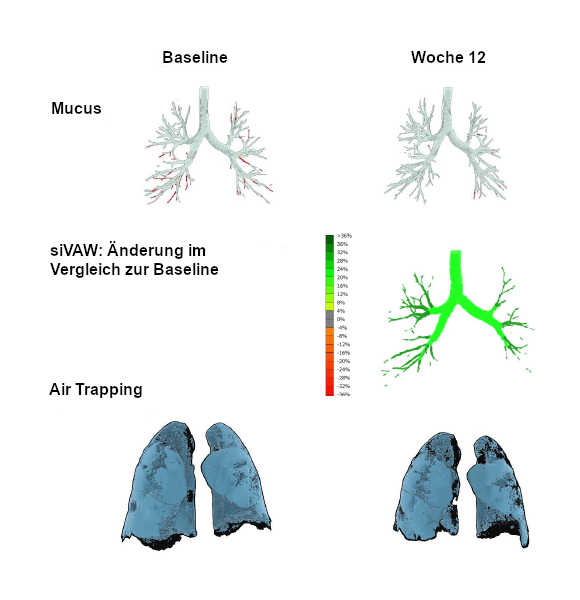
Wie schnell die Verbesserung der Asthmasymptome bei SEA-Patient:innen unter Fasenra®* einsetzt, verdeutlicht eindrucksvoll eine kürzlich auf dem Kongress der European Respiratory Society (ERS) vorgestellte Beobachtungsstudie: Bereits 12 Wochen nach Therapiestart kam es zu einer signifikanten Reduktion der Mucus Plugs und des Air Trappings in der Lunge sowie zu einer Erhöhung des Atemwegvolumens** im Vergleich zur Baseline, wie beispielhaft an den Ergebnissen eine:r individuellen Patient:in in der folgenden Abbildung zu sehen ist.3
|
|
|
Lesen Sie weiter für mehr Informationen zur Studie.
Eosinophile, Mucus Plugs und Atemwegsobstruktion4
|
•
|
Mucus Plugs treten bei mehr als der Hälfte der Asthma-Patient:innen auf und sind ein möglicher Mechanismus der chronischen Atemwegsobstruktion bei schwerem Asthma.
|
|
•
|
Sie sind assoziiert mit niedrigerer Einsekundenkapazität (FEV1) sowie einer erhöhten Zahl an Eosinophilen und eosinophiler Peroxidase (EPO) im Sputum.
|
|
•
|
EPO-generierte Oxidantien könnten an der Entstehung von Mucus Plugs beteiligt sein.
|
|
Die Daten im Detail
Die Beobachtungsstudie von Conemans et al. untersuchte den unmittelbaren Einfluss von Fasenra® auf die Atemwegspathologie bei 20 Patient:innen mit schwerem eosinophilen Asthma mittels funktioneller Bildgebung (Functional Respiratory Imaging, FRI).*,3 Die Datenbasis: hochauflösende Computertomografie-Scans (HRCT) der funktionellen Residualkapazität (FRC) und der totalen Lungenkapazität (TLC).
Nach 12 Wochen unter Fasenra® zeigte sich:3
|
•
|
eine signifikante Reduktion des Mucus Scores (–0,41 Punkte; p < 0,01) vs. Baseline und
|
|
•
|
eine signifikante Reduktion des Air Trappings (–5,47 Punkte; p < 0,01) vs. Baseline.
|
|
•
|
Je weniger Mucus, desto besser die FEV1: Mit jedem Punkt, um den der Mucus Score reduziert wurde, stieg der FEV1-Wert um 1,33 %.
|
|
•
|
Darüber hinaus wurden signifikante Verbesserungen des Atemwegsvolumens** und des Residualvolumens vs. Baseline (+14 % bzw. +27 %; jeweils p = 0,02) beobachtet.
|
Die FRI machte eindrucksvoll sichtbar, wie Veränderungen der Mucus Plugs auf die Lungenfunktion wirkte – und welche Verbesserungen unter Fasenra® möglich waren.3

|
|
Fachinformation Fasenra®.
DE-76604/11-24
|
|
* Fasenra® ist angezeigt als Add-on-Erhaltungstherapie bei erwachsenen Patient:innen mit schwerem eosinophilem Asthma, das trotz hochdosierter inhalativer Corticosteroide plus lang wirksamer Beta-Agonisten unzureichend kontrolliert ist.
** gemessen am specific image-based airway volume, kurz siVAW
|
|
1.
|
Lommatzsch M, Criee CP, De Jong C, et al. S2k-Leitlinie zur fachärztlichen Diagnostik und Therapie von Asthma 2023. Online verfügbar unter: https://register.awmf.org/assets/guidelines/020-009l_S2k_Fachaerztliche-Diagnostik-Therapie-von-Asthma_2023-03.pdf (letzter Zugriff: Oktober 2024).
|
|
2.
|
Fachinformation Fasenra®. Stand Oktober 2024.
|
|
3.
|
Conemans L et al. Effect of benralizumab on airway mucus, air-trapping and airway volume assessed by functional respiratory imaging in severe eosinophilic asthma. Poster 5367. Präsentiert auf dem ERS-Kongress 2024, 7.-11. September 2024.
|
|
4.
|
Dunican EM, Elicker BM, Gierada DS, et al. Mucus plugs in patients with asthma linked to eosinophilia and airflow obstruction. J Clin Invest 2018;128(3):997–1009.
|
|
|
Fasenra® 30 mg Injektionslösung in einer Fertigspritze
Fasenra® 30 mg Injektionslösung im Fertigpen
Wirkstoff: Benralizumab. Verschreibungspflichtig. Zusammensetzung: Jede Fertigspritze/jeder Fertigpen enthält 30 mg Benralizumab in 1 ml. Benralizumab ist ein humanisierter monoklonaler Antikörper, der mittels rekombinanter DNA-Technologie in Ovarialzellen des chinesischen Hamsters hergestellt wird. Sonstige Bestandteile: Histidin, Histidinhydrochlorid-Monohydrat, Trehalose-Dihydrat (Ph.Eur.), Polysorbat 20 (E 432), Wasser für Injektionszwecke. Anwendungsgebiete: Asthma: Fasenra ist angezeigt als Add-on-Erhaltungstherapie bei erwachsenen Patienten mit schwerem eosinophilem Asthma, das trotz hochdosierter inhalativer Corticosteroide plus lang wirksamer Beta-Agonisten unzureichend kontrolliert ist (siehe 5.1 der Fachinformation). Eosinophile Granulomatose mit Polyangiitis (EGPA): Fasenra ist angezeigt als Add-on-Therapie bei erwachsenen Patienten mit rezidivierender oder refraktärer eosinophiler Granulomatose mit Polyangiitis (siehe 5.1 der Fachinformation). Gegenanzeigen: Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile. Nebenwirkungen: Häufig: Pharyngitis, Überempfindlichkeitsreaktionen, Kopfschmerzen, Fieber, Reaktion an der Injektionsstelle; Nicht bekannt: Anaphylaktische Reaktion. Weitere Hinweise: siehe Fachinformation. Pharmazeutischer Unternehmer: AstraZeneca GmbH, Friesenweg 26, 22763 Hamburg, E-Mail: [email protected], www.astrazeneca.de, Servicehotline für Produktanfragen: 0800 22 88 660.
Stand: Q4 2024.
DE-75624/2024
|
|

|
|
|

|
„Kompakt Pneumologie“ ist ein Titel der Biermann Verlag GmbH in Köln. Sie erhalten diese E-Mail, da Sie für diesen Newsletter angemeldet sind. Sie können in unserem Fachportal weitere Newsletter zu verschiedenen medizinischen Fachrichtungen abonnieren. Sollten Sie kein Interesse mehr an diesem Newsletter haben, können Sie sich hier abmelden. Haben Sie Fragen oder Anregungen zu unseren Themen und Inhalten, freuen wir uns auf Ihre E-Mail: [email protected]. Bitte beachten Sie, dass dieser Newsletter nur Angehörigen der Heilberufe gemäß HWG §10 zugänglich gemacht werden darf; das gilt auch für das Weiterempfehlen und Weiterleiten.
Impressum: Biermann Verlag GmbH | MedCon Health Contents GmbH | HRB Bonn 11110 | HRB Köln 78926
Geschäftsführer: Dr. med. Hans Biermann
Hier vollständiges Impressum aufrufen
|
|
|
|
|