|
Nahezu vollständige Entfernung der Eosinophile dank einzigartigem Wirkmechanismus

|
|
Liebe Leser:innen,
es gibt eine Vielzahl von eosinophil getriebenen Erkrankungen.1 Bei Asthma sind Eosinophile an Prozessen beteiligt, die u. a. zu einem Remodeling der Atemwege und zur Obstruktion des Luftstroms beitragen können. Hierzu zählen Epithelschäden, Hypertrophie der glatten Muskulatur, neuronale Plastizität und beeinträchtigte Gewebereparaturprozesse.2 Darüber hinaus sind Eosinophile auch an seltenen Erkrankungen wie eosinophiler Granulomatose mit Polyangiitis (EGPA) beteiligt und fördern multisystemische Organschäden und Dysfunktionen.2

Fasenra® greift direkt an den Eosinophilen an
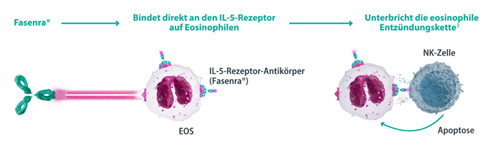
Fasenra® hat sich aufgrund seiner einzigartigen Wirkweise bei der Therapie des unkontrollierten schweren eosinophilen Asthmas bewährt:*,3 Es bindet direkt an den IL-5-Rezeptor auf den Eosinophilen und unterbricht so die eosinophile Entzündungskette.3 Innerhalb von 24 Stunden nach der ersten Dosis werden die Eosinophilen nahezu vollständig reduziert – und das nachhaltig.3 Zuletzt wiesen Versorgungsdaten auf die starke und anhaltende Wirkung des Anti-IL-5-R-Antikörpers hin: In der BenRex-Studie traten über einen Zeitraum von bis zu 18 Monaten unter Fasenra® keine eosinophil getriebenen Exazerbationen auf.**,4
|
Der duale Wirkansatz von Fasenra® auf einen Blick
|
•
|
Inhibition der Signaltransduktion von IL-5, einem proinflammatorischen Schlüsselzytokin beim schweren eosinophilen Asthma3,5,6
|
|
•
|
Rekrutierung von Immuneffektorzellen, die zytotoxisch auf Eosinophile wirken3
|
|
•
|
Induzierte antikörperabhängige zellvermittelte Zytotoxizität (ADCC) leitet die Apoptose von Eosinophilen und Basophilen ein3
|
|
•
|
Ermöglicht nahezu vollständigen Stopp der eosinophilen Entzündungskette innerhalb von 24 h nach der ersten Dosis3
|
|
•
|
Einziger zugelassener Antikörper gegen den IL-5-Rezeptor auf eosinophilen Granulozyten
|
|

Fasenra® bei EGPA: Remission mit gleichzeitiger OCS-Reduktion
Seit November 2024 ist Fasenra® auch zur Behandlung von rezidivierter oder refraktärer EGPA*** zugelassen.3 Basis für die Zulassung war die MANDARA-Studie, eine Nicht-Unterlegenheitsstudie und der erste direkte Head-to-head-Vergleich der Wirksamkeit und Verträglichkeit von Fasenra® vs. Mepolizumab bei EGPA.7 Alle in die Studie eingeschlossenen Patient:innen hatten auch Asthma.7
|
Unter Fasenra®
|
|
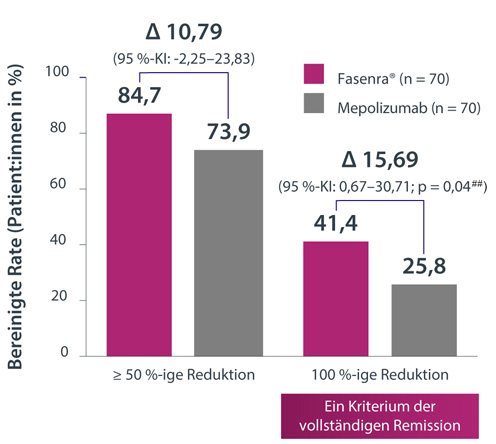
… erreichten 58 % der Patient:innen die EGPA-Remission# in Woche 36 und 48 (vs. 57 % unter Mepolizumab; primärer Endpunkt).§,3
|
|
|
… konnten EGPA-Patient:innen in den Wochen 48 bis 52 in nominal signifikant größerem Ausmaß OCS vollständig absetzen, im Vergleich zu Mepolizumab (sekundärer Endpunkt).§§,3,7
|
|

|
|
Fachinformation Fasenra®.
DE-78377/01-25
|
|
* Fasenra® ist angezeigt als Add-on-Erhaltungstherapie bei erwachsenen Patient:innen mit schwerem eosinophilem Asthma, das trotz hochdosierter inhalativer Corticosteroide plus lang wirksamer Beta-Agonisten unzureichend kontrolliert ist.3
** BenRex: prospektive Beobachtungsstudie (UK), die inflammatorische und physiologische Merkmale von Asthma-Exazerbationen unter Benralizumab-Therapie untersuchte. Eingeschlossen waren 156 Patient:innen unter Benralizumab-Therapie.4
*** Fasenra® ist angezeigt als Add-on-Therapie bei erwachsenen Patient:innen mit rezidivierender oder refraktärer eosinophiler Granulomatose mit Polyangiitis.3
# Die Definition für Remission kann je nach Quelle variieren. MANDARA-/MIRRA-Kriterien: BVAS = 0, Kortison ≤ 4,0 mg Tag, EULAR-Kriterien: BVAS = 0, OCS ≤ 7,5 mg Tag
## Nominale Signifikanz.
§ Δ 1,21 % (95 %-KI: -14,12–16,53; p = 0,88 für Überlegenheit).3 Fasenra® zeigte gegenüber Mepolizumab im primären Endpunkt eine Nicht-Unterlegenheit, da der untere Grenzwert des 95 %-Konfidenzintervalls über 25 % lag.7
§§ Die OCS- wurde als Tagesdosis von Prednison oder Prednisolon berechnet, unabhängig vom Grund der Verabreichung. Bei Patient:innen, die vor Woche 52 aus der Studie ausschieden, wurde die OCS-Dosis in den vorangegangenen 28 Tagen als Grundlage zur Ableitung der mittleren Tagesdosis und prozentualen Dosisreduktion gegenüber dem Ausgangswert in den Wochen 48 bis 52 verwendet. Patient:innen, die die Behandlung vor Woche 48 abbrachen, wurden bei der Analyse der prozentualen Dosisreduktion als nicht ansprechend betrachtet.7
EGPA: eosinophile Granulomatose mit Polyangiitis; IL-5: Interleukin-5; OCS: orale Corticosteroide
Referenzen
|
|
1.
|
Gandhi NA et al. Nat Rev Drug Discov 2016;15(1):35–50.
|
|
2.
|
Wechsler ME et al. Mayo Clin Proc 2021;96(10):2694–707.
|
|
3.
|
Fachinformation Fasenra®. Stand Oktober 2024.
|
|
4.
|
Logan J et al. Asthma Exacerbation Profile on open label treatment with Benralizumab for severe eosinophilic asthma [BenRex]. Poster 5356. Präsentiert auf dem ERS-Kongress 2024, 7.-11. September 2024.
|
|
5.
|
Ghazi A et al. Expert Opin Biol Ther 2012;12(1):113–8.
|
|
6.
|
Tan L et al. J Asthma Allergy 2016;71.
|
|
7.
|
Wechsler ME et al. N Engl J Med 2024;doi: 10.1056/NEJMoa2311155.
|
|
|
Fasenra® 30 mg Injektionslösung in einer Fertigspritze
Fasenra® 30 mg Injektionslösung im Fertigpen
Wirkstoff: Benralizumab. Verschreibungspflichtig. Zusammensetzung: Jede Fertigspritze/jeder Fertigpen enthält 30 mg Benralizumab in 1 ml. Benralizumab ist ein humanisierter monoklonaler Antikörper, der mittels rekombinanter DNA-Technologie in Ovarialzellen des chinesischen Hamsters hergestellt wird. Sonstige Bestandteile: Histidin, Histidinhydrochlorid-Monohydrat, Trehalose-Dihydrat (Ph.Eur.), Polysorbat 20 (E 432), Wasser für Injektionszwecke. Anwendungsgebiete: Asthma: Fasenra ist angezeigt als Add-on-Erhaltungstherapie bei erwachsenen Patienten mit schwerem eosinophilem Asthma, das trotz hochdosierter inhalativer Corticosteroide plus lang wirksamer Beta-Agonisten unzureichend kontrolliert ist (siehe 5.1 der Fachinformation). Eosinophile Granulomatose mit Polyangiitis (EGPA): Fasenra ist angezeigt als Add-on-Therapie bei erwachsenen Patienten mit rezidivierender oder refraktärer eosinophiler Granulomatose mit Polyangiitis (siehe 5.1 der Fachinformation). Gegenanzeigen: Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile. Nebenwirkungen: Häufig: Pharyngitis, Überempfindlichkeitsreaktionen, Kopfschmerzen, Fieber, Reaktion an der Injektionsstelle; Nicht bekannt: Anaphylaktische Reaktion. Weitere Hinweise: siehe Fachinformation. Pharmazeutischer Unternehmer: AstraZeneca GmbH, Friesenweg 26, 22763 Hamburg, E-Mail: [email protected], www.astrazeneca.de, Servicehotline für Produktanfragen: 0800 22 88 660.
Stand: Q4 2024.
DE-75624/2024
|
| |

|
|
| |
|
„Kompakt Pneumologie“ ist ein Titel der Biermann Verlag GmbH in Köln. Sie erhalten diese E-Mail, da Sie für diesen Newsletter angemeldet sind. Sie können in unserem Fachportal weitere Newsletter zu verschiedenen medizinischen Fachrichtungen abonnieren. Sollten Sie kein Interesse mehr an diesem Newsletter haben, können Sie sich hier abmelden. Haben Sie Fragen oder Anregungen zu unseren Themen und Inhalten, freuen wir uns auf Ihre E-Mail: [email protected]. Bitte beachten Sie, dass dieser Newsletter nur Angehörigen der Heilberufe gemäß HWG §10 zugänglich gemacht werden darf; das gilt auch für das Weiterempfehlen und Weiterleiten.
Impressum: Biermann Verlag GmbH | MedCon Health Contents GmbH | HRB Bonn 11110 | HRB Köln 78926
Geschäftsführer: Dr. med. Hans Biermann
Hier vollständiges Impressum aufrufen
|
|
|
|
|