

|
Liebe Leserinnen und Leser,
der kürzlich veröffentlichte GOLD-Report 2025 bringt bedeutende Neuerungen in der Therapie
der chronisch obstruktiven Lungenerkrankung (COPD) mit sich. Besonders hervorzuheben ist
die Aufnahme von Dupilumab (DUPIXENT®) als erstes Biologikum in den
Therapiealgorithmus.1 Diese Entwicklung markiert einen Meilenstein
in der Behandlung von COPD-Patienten# mit Typ-2-Inflammation.
DUPIXENT®: Ein neues Kapitel in der COPD-Therapie
DUPIXENT® wirkt, indem es die Signalwege von Interleukin-4
und Interleukin-13 blockiert, die zentrale Treiber der Typ-2-Inflammation
sind.2,3 Diese Typ-2-Inflammation kann bei 20–40 % der COPD-Patienten
zugrunde liegen.4 Der monoklonale Antikörper, DUPIXENT®
wurde von der EMA im Juni 2024 für die Behandlung von Erwachsenen mit unkontrollierter COPD mit
erhöhten Blut-Eosinophilenwerten (EOS ≥ 300/µl) zugelassen, die trotz Triple-Therapie oder dualer
Therapie (wenn ICS nicht angebracht) weiterhin unter Exazerbationen leiden.**,5
|

|
Der GOLD-Report 2025 nimmt DUPIXENT® (Dupilumab) als Folgebehandlung bei
Patienten mit folgenden Kriterien auf:1
|
|
|
|
|
•
|
Exazerbationen trotz maximaler inhalativer Therapie,
|
|
•
|
Erhöhte EOS-Werte (≥ 300/µl), und
|
|
•
|
Symptome einer chronischen Bronchitis.
|
|
|

|
|
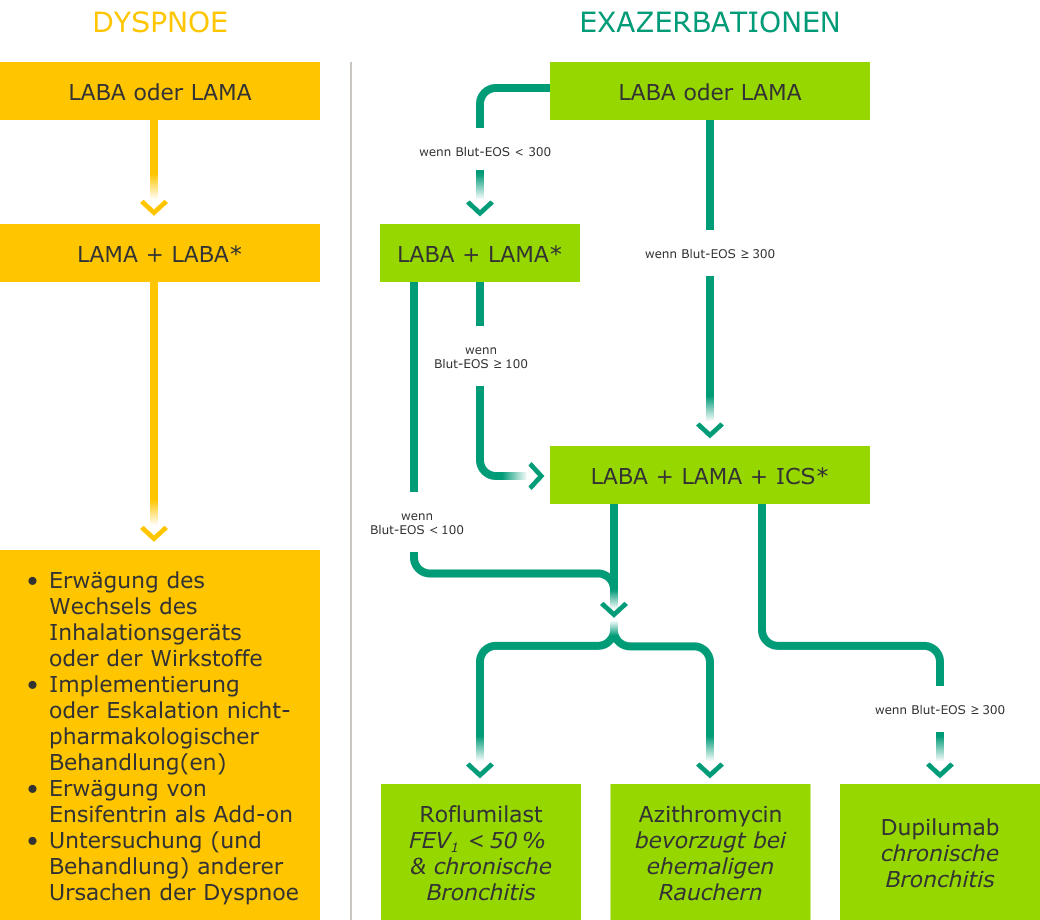
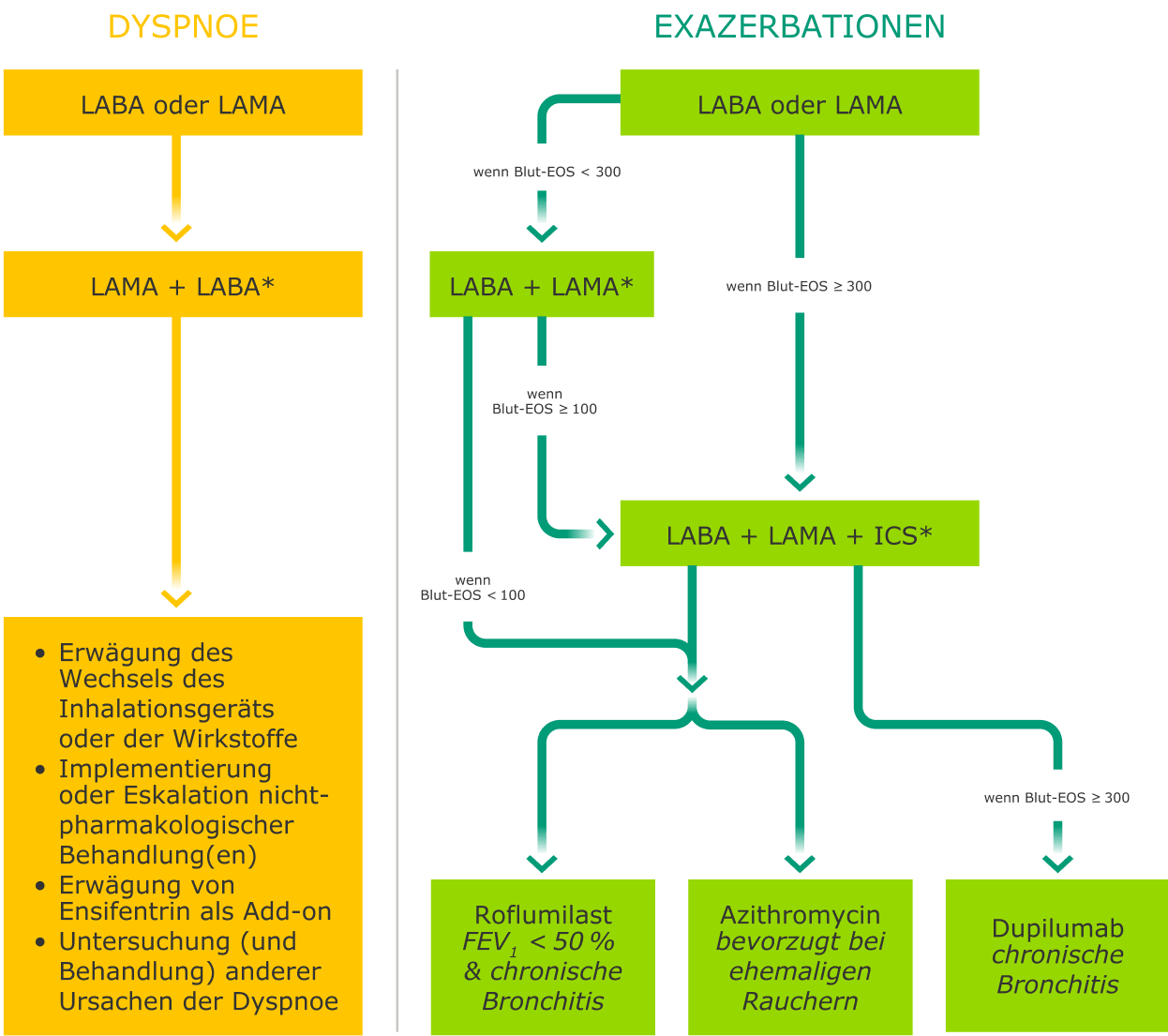
Pharmakologische Folgebehandlung1
|
|
* Eine Behandlung mit einem einzigen Inhalator kann einfacher und wirksamer
sein als mehrere Inhalatoren. Die Verwendung eines einzigen Inhalators verbessert die Therapietreue.
Bei Pneumonie oder anderen erheblichen Nebenwirkungen ist eine Deeskalation der ICS in Betracht zu ziehen.
Bei EOS-Werten im Blut ≥ 300/μl ist eine Deeskalation eher mit der Entwicklung von Exazerbationen verbunden.
Exazerbationen beziehen sich auf die Anzahl der Exazerbationen pro Jahr.
© 2024, 2025 Global Strategy for Diagnosis, Management and Prevention of COPD, all rights reserved.
Use is by express license from the owner.
|
|
|
Ensifentrin und Azithromycin sind in Deutschland nicht für die Behandlung der COPD zugelassen (Stand Januar 2025).
|
|
Die Aufnahme von DUPIXENT® in den GOLD-Report 2025 stellt einen Paradigmenwechsel
dar.1 Erstmals steht ein Biologikum zur Verfügung, das gezielt auf eine spezifische
Entzündungsform bei COPD abzielt.5 Dies eröffnet neue Perspektiven für Patienten
mit Typ-2-Inflammation, bei denen herkömmliche Therapien oft nicht ausreichen.
|
|
|
|
|

|
|
Für Patienten mit anhaltenden Symptomen trotz inhalativer Triple-Therapieb
|
|
Eine innovative Therapie bei COPD mit erhöten EOS-Werten im Blut (≥ 300/μl)**,5
|


|
|
BD = Bronchodilatatorengabe;
COPD = chronisch obstruktive Lungenerkrankung;
EOS = eosinophile Granulozyten;
FEV1 = Einsekundenkapazität;
ICS = inhalative Kortikosteroide;
IL = Interleukin;
KI = Konfidenzintervall;
LABA = langwirksame Beta-2-Sympathomimetika;
LAMA = langwirksame Muskarinantagonisten;
LS = Methode der kleinsten Quadrate (least squares);
SGRQ = St. George’s Respiratory Questionnaire.
** DUPIXENT® ist angezeigt als Add-on-Erhaltungstherapie bei erwachsenen Patienten mit durch eine erhöhte Anzahl an Eosinophilen im Blut gekennzeichneter chronisch obstruktiver Lungenerkrankung (COPD), die trotz einer Kombinationstherapie aus LAMA/LABA/ICS oder, falls ICS nicht angebracht ist, einer Kombinationstherapie aus LAMA/LABA unzureichend kontrolliert ist.f,5 |
# Allein aus Gründen der besseren Lesbarkeit wurde auf die gleichzeitige Verwendung geschlechtsspezifischer Sprachformen verzichtet. Sämtliche Personenbezeichnungen gelten aber selbstverständlich für alle Geschlechter. |
a Chronische Bronchitis ist nicht Teil des Zulassungslabels von DUPIXENT®. Der Anteil der Patienten mit Emphysem in den Zulassungsstudien betrug ca. 30 %.5–7 |
b LAMA/LABA/ICS (97,6 % der Patienten der BOREAS-Studie, 98,8 % der Patienten der NOTUS-Studie) oder nur LAMA/LABA, falls ICS nicht angebracht (2,4 % der Patienten der BOREAS-Studie, 1,2 % der Patienten der NOTUS-Studie)6,7 |
c In der 52. Woche der NOTUS-Studie kam es bei den DUPIXENT®-Patienten zu einer annualisierten Rate von 0,86 mittelschweren oder schweren Exazerbationeng und von 1,30 bei den Placebopatienten. Das Ratenverhältnis gegenüber Placebo betrug 0,66 (95 %-KI: 0,54–0,82; p < 0,001; primärer Endpunkt).7 |
d Verbesserung der Lungenfunktion in Woche 12 der BOREAS-Studie um 160 ml vs. Baseline (LS-Mittelwert) und 83 ml vs. Placebo (LS-Mittelwertdifferenz) (p < 0,001; sekundärer Endpunkt); der Unterschied wurde bereits in Woche 2 beobachtet und hielt bis Woche 52 (83 ml LS-Mittelwertdifferenz; p < 0,001) an.6 |
e 51,5 % der DUPIXENT®-Patienten erreichten in Woche 52 der BOREAS-Studie eine Verbesserung des SGRQ-Gesamtscores um ≥ 4 Punkte gegenüber 43,1 % der Placebopatienten (p = 0,009; sekundärer Endpunkt) bei einer durchschnittlichen Verbesserung vs. Baseline von 9,7 Punkten unter DUPIXENT® und 6,4 Punkten unter Placebo (LS-Mittelwertdifferenz: –3,4; 95 %-KI: –5,5 bis –1,3; p = 0,002; sekundärer Endpunkt).6 |
f In den Zulassungsstudien BOREAS und NOTUS waren Patienten mit EOS ≥ 300/μl eingeschlossen. Unzureichende Kontrolle war gekennzeichnet durch ≥ 2 mittelschwere oder ≥ 1 schwere Exazerbation im Jahr zuvor, mindestens eine Exazerbation unter inhalativer Triple-Therapie (bzw. unter LAMA/LABA, falls ICS nicht angebracht).6,7 |
g Mittelschwere Exazerbationen wurden definiert als Exazerbationen, die zu einer Behandlung mit systemischen Kortikosteroiden, einem Antibiotikum oder beidem führten. Schwere Exazerbationen wurden definiert als Exazerbationen, die zu einem Krankenhausaufenthalt, dem Aufsuchen der Notaufnahme oder zum Tod führten.7
1. GOLD. Global Initiative for Chronic Obstructive Lung Disease 2025. https://goldcopd.org/wp-content/uploads/2024/11/GOLD-2025-Report-v1.0-15Nov2024_WMV.pdf (letzter Zugriff: Februar 2025);
2. Gandhi NA et al. Nat Rev Drug Discov 2016; 15(1): 35–50;
3. Garudadri S, Woodruff PG. Ann Am Thorac Soc 2018; 15(Suppl 4): S234–S238;
4. Rabe KF et al. Am J Respir Crit Care Med 2023; 208(4): 395–405;
5. DUPIXENT® Fachinformation, aktueller Stand;
6. Bhatt SP et al. N Engl J Med 2023; 389(3): 205–214; inkl. Supplement;
7. Bhatt SP et al. N Engl J Med 2024; 390(24): 2274–2283; inkl. Supplement.
|
|
|

|
MAT-DE-2500622-1.0-02/2025
© Sanofi 2025. Alle Rechte vorbehalten
Datenschutz |
Nutzungsbedingungen |
Kontakt |
Impressum
Sanofi-Aventis Deutschland GmbH · Lützowstraße 107 · D-10785 Berlin
· Telefon +49 (0) 30 2575 2000
· Fax +49 (0) 30 2575 2001
· www.sanofi.de
Sitz der Gesellschaft: Frankfurt am Main – Handelsregister: Frankfurt am Main, Abt. B Nr. 40661
Vorsitzender des Aufsichtsrates: Brendan O’Callaghan – Geschäftsführer: Heidrun Irschik-Hadjieff (Vorsitzende),
Oliver Coenenberg, Dr. Peter Naumann, Anne Reuschenbach, Dr. Marion Zerlin
|
|
|
|
|
„Kompakt Pneumologie“ ist ein Titel der Biermann Verlag GmbH in Köln. Sie erhalten diese E-Mail, da Sie für diesen Newsletter angemeldet sind. Sie können in unserem Fachportal weitere Newsletter zu verschiedenen medizinischen Fachrichtungen abonnieren. Sollten Sie kein Interesse mehr an diesem Newsletter haben, können Sie sich hier abmelden. Haben Sie Fragen oder Anregungen zu unseren Themen und Inhalten, freuen wir uns auf Ihre E-Mail: [email protected]. Bitte beachten Sie, dass dieser Newsletter nur Angehörigen der Heilberufe gemäß HWG §10 zugänglich gemacht werden darf; das gilt auch für das Weiterempfehlen und Weiterleiten.
Impressum: Biermann Verlag GmbH | MedCon Health Contents GmbH | HRB Bonn 11110 | HRB Köln 78926
Geschäftsführer: Dr. med. Hans Biermann
Hier vollständiges Impressum aufrufen
|
|
|
|
|
|