|
Jetzt Neuigkeiten erfahren!

|
|
Liebe Leser:innen,
die Jahrestagung der American Thoracic Society (ATS) Ende Mai bot zahlreiche Einblicke zur Therapie von eosinophiler Granulomatose mit Polyangiitis (EGPA). EGPA ist eine seltene, systemische Vaskulitis, die durch eine erhöhte Anzahl eosinophiler Granulozyten (EOS) gekennzeichnet ist.1 EOS spielen auch bei Asthma eine zentrale Rolle, insbesondere bei schwerem eosinophilen Asthma.2 Nahezu alle EGPA-Patient:innen haben auch Asthma, viele von ihnen schweres Asthma.3,4
Fasenra® kann sowohl für die Behandlung von schwerem eosinophilen Asthma* als auch bei rezidivierender oder refraktärer EGPA** eingesetzt werden.5 Auch zu Fasenra® bei EGPA wurden auf dem ATS neue Daten vorgestellt.

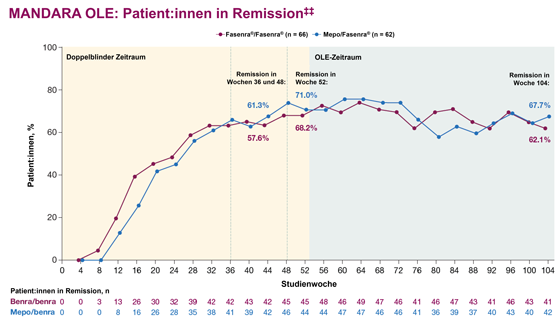
Open-label-Extension der MANDARA-Studie: EGPA-Remission unter Fasenra® bleibt über 2 Jahre erhalten
Die MANDARA-Studie ist die erste Head-to-head-Nicht-Unterlegenheitsstudie von Fasenra® und Mepolizumab bei EGPA.6 Nach Ende der 52-wöchigen, doppelblinden Studienphase wechselten die Patient:innen, die vorher Mepolizumab erhalten hatten, zu Fasenra®**. Erste Daten aus dieser Open-label-Extension wurden auf der ATS-Jahrestagung vorgestellt. Sie zeigten in beiden Studienarmen (Fasenra®/Fasenra® und Mepolizumab/Fasenra®):7,‡
|
•
|
Die Remission‡‡ blieb über 2 Jahre erhalten# (siehe Abbildung).
|
|
•
|
Jeweils 44 % der Patient:innen konnten in den Wochen 101–104 komplett auf orale Corticosteroide (OCS) verzichten.
|
|
•
|
Die EOS im Blut wurden nahezu vollständig reduziert.
|
|
•
|
Bei Patient:innen, die von Mepolizumab auf Fasenra® umgestellt wurden, kam es zu einer zusätzlichen Reduktion der Blut-EOS sowie einer zusätzlichen OCS-Reduktion.
|
|

Analysen aus dem englischen Versorgungsalltag unterstreichen den Bedarf an effektiven EGPA-Therapien
Zwei retrospektive Beobachtungsstudien aus England untersuchten den Krankheitsstatus (Remission, Rezidiv oder stabile Erkrankung) und den Gebrauch von Ressourcen des Gesundheitssystems in Abhängigkeit des Krankheitsstatus.8,9 Eingeschlossen waren jeweils 486 EGPA-Patient:innen; der durchschnittliche Follow-up-Zeitraum betrug 5,4 Jahre.8,9 Die wichtigsten Ergebnisse:
|
•
|
Viele EGPA-Patient:innen erreichten keine Remission##: Der Anteil der Patient:innen, die eine Remission erreichten, war über einen durchschnittlichen Follow-up-Zeitraum von 5,4 Jahren gering.8
|
|
•
|
Zudem konnten 60 % der Patient:innen, die eine Remission## erreichten, diese nicht erhalten.8
|
|
•
|
Die Kosten für das Gesundheitssystem waren bei Patient:innen in Remission## deutlich geringer als bei Patient:innen, die nicht in Remission waren.9
|
Aktualisierte Fasenra®-Website mit neuen Infos zu EGPA entdecken
Ab sofort finden Sie dort nicht nur detaillierte Informationen zur Wirksamkeit und Verträglichkeit von Fasenra® bei schwerem eosinophilen Asthma*, sondern auch zum Einsatz bei rezidivierender oder refraktärer EGPA**.
Zudem haben Sie die Möglichkeit, hilfreiches Informationsmaterial direkt herunterzuladen.

|
|
Fachinformation Fasenra®.
DE-83511/06-25
|
|
* Fasenra ist angezeigt als Add-on-Erhaltungstherapie bei erwachsenen Patient:innen mit schwerem eosinophilem Asthma, das trotz hochdosierter inhalativer Corticosteroide plus lang wirksamer Beta-Agonisten unzureichend kontrolliert ist.5
** Fasenra® ist angezeigt als Add-on-Therapie bei erwachsenen Patient:innen mit rezidivierender oder refraktärer eosinophiler Granulomatose mit Polyangiitis.5
‡ Mepolizumab wurde nur für 1 Jahr gegeben. Daher ist ein direkter Vergleich zwischen einer 2-jährigen Gabe von Fasenra® vs. Mepolizumab nicht möglich.
‡‡ Remission war definiert als BVAS = 0 und OCS ≤4 mg/Tag.
# Von den Patient:innen, die in Woche 24 eine Remission erreichten, blieben unter Fasenra®/Fasenra® 48,3 % und unter Mepolizumab/Fasenra 55,2 % der Patient:innen bis Woche 104 in Remission.
## Remission war definiert als keine neuen EGPA-Ereignisse, Asthma-Exazerbationen oder Nasenpolypen in den letzten 6 Monaten und OCS ≤4 mg/Tag.
EGPA: eosinophile Granulomatose mit Polyangiitis; IL-5: Interleukin-5; OCS: orale Corticosteroide
Referenzen
|
|
1.
|
Furuta S et al. Allergol Int 2019;68(4):430–6.
|
|
2.
|
Wechsler ME et al. Mayo Clin Proc 2021;96(10):2694–707.
|
|
3.
|
Trivioli G et al. Rheumatology 2020;59(Suppl 3):iii84–94.
|
|
4.
|
Cottin V et al. Eur Respir J 2016;48(5):1429–41.
|
|
5.
|
Fachinformation Fasenra®. Stand Oktober 2024.
|
|
6.
|
Wechsler ME et al. N Engl J Med 2024;390:911–21.
|
|
7.
|
Wechsler ME et al. Two-year efficacy and safety of benralizumab for the treatment of eosinophilic granulomatosis with polyangiitis. Präsentiert auf dem ATS 2025. Poster 1008.
|
|
8.
|
Siddiqui SH et al. Disease states in patients with eosinophilic granulomatosis with polyangiitis (EGPA) in England: a retrospective observational cohort study. Präsentiert auf dem ATS 2025. Poster P47.
|
|
9.
|
Siddiqui SH et al. Healthcare resource utilization and associated costs across three health states in patients with eosinophilic granulomatosis with polyangiitis (EGPA): a retrospective observational cohort study in England. Präsentiert auf dem ATS 2025. Poster P48.
|
|
|
Fasenra® 30 mg Injektionslösung in einer Fertigspritze
Fasenra® 30 mg Injektionslösung im Fertigpen
Wirkstoff: Benralizumab. Verschreibungspflichtig. Zusammensetzung: Jede Fertigspritze/jeder Fertigpen enthält 30 mg Benralizumab in 1 ml. Benralizumab ist ein humanisierter monoklonaler Antikörper, der mittels rekombinanter DNA-Technologie in Ovarialzellen des chinesischen Hamsters hergestellt wird. Sonstige Bestandteile: Histidin, Histidinhydrochlorid-Monohydrat, Trehalose-Dihydrat (Ph.Eur.), Polysorbat 20 (E 432), Wasser für Injektionszwecke. Anwendungsgebiete: Asthma: Fasenra ist angezeigt als Add-on-Erhaltungstherapie bei erwachsenen Patienten mit schwerem eosinophilem Asthma, das trotz hochdosierter inhalativer Corticosteroide plus lang wirksamer Beta-Agonisten unzureichend kontrolliert ist (siehe 5.1 der Fachinformation). Eosinophile Granulomatose mit Polyangiitis (EGPA): Fasenra ist angezeigt als Add-on-Therapie bei erwachsenen Patienten mit rezidivierender oder refraktärer eosinophiler Granulomatose mit Polyangiitis (siehe 5.1 der Fachinformation). Gegenanzeigen: Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile. Nebenwirkungen: Häufig: Pharyngitis, Überempfindlichkeitsreaktionen, Kopfschmerzen, Fieber, Reaktion an der Injektionsstelle; Nicht bekannt: Anaphylaktische Reaktion. Weitere Hinweise: siehe Fachinformation. Pharmazeutischer Unternehmer: AstraZeneca GmbH, Friesenweg 26, 22763 Hamburg, E-Mail: [email protected], www.astrazeneca.de, Servicehotline für Produktanfragen: 0800 22 88 660.
Stand: Q4 2024.
DE-75624/2024
|
| |

|
|
| |
|
„Kompakt Pneumologie“ ist ein Titel der Biermann Verlag GmbH in Köln. Sie erhalten diese E-Mail, da Sie für diesen Newsletter angemeldet sind. Sie können in unserem Fachportal weitere Newsletter zu verschiedenen medizinischen Fachrichtungen abonnieren. Sollten Sie kein Interesse mehr an diesem Newsletter haben, können Sie sich hier abmelden. Haben Sie Fragen oder Anregungen zu unseren Themen und Inhalten, freuen wir uns auf Ihre E-Mail: [email protected]. Bitte beachten Sie, dass dieser Newsletter nur Angehörigen der Heilberufe gemäß HWG §10 zugänglich gemacht werden darf; das gilt auch für das Weiterempfehlen und Weiterleiten.
Impressum: Biermann Verlag GmbH | MedCon Health Contents GmbH | HRB Bonn 11110 | HRB Köln 78926
Geschäftsführer: Dr. med. Hans Biermann
Hier vollständiges Impressum aufrufen
|
|
|
|
|