|
Mit Serplulimab (HETRONIFLY®) ist in Europa seit Februar 2025 der erste Anti-PD-1-Antikörper für die Erstlinientherapie des fortgeschrittenen kleinzelligen Bronchialkarzinoms (SCLC) in Kombination mit Carboplatin und Etoposid zugelassen.1,2
Lebensqualität unter Serplulimab zum Teil verbessert
Ergebnisse der doppelblinden, placebokontrollierten Phase-III-Studie ASTRUM-005 zeigten, dass die gesundheitsbezogene Lebensqualität (HRQoL) unter Therapie mit Serplulimab plus Chemotherapie erhalten blieb. Demnach zeigte sich in insgesamt 7 Symptomdomänen in einer Fragebogen-gestützten Post-hoc-Analyse auf Basis des QLQ-C30 (funktional und symptomatisch) sowie des QLQ-LC30 (symptomatisch) 18 Wochen nach Baseline eine Verbesserung:3
- Husten
- Hämoptyse
- Dyspnoe
- Dysphagie
- Schmerzen in Armen/Schultern
- Schmerzen in der Brust
- Schmerzen in anderen Körperteilen
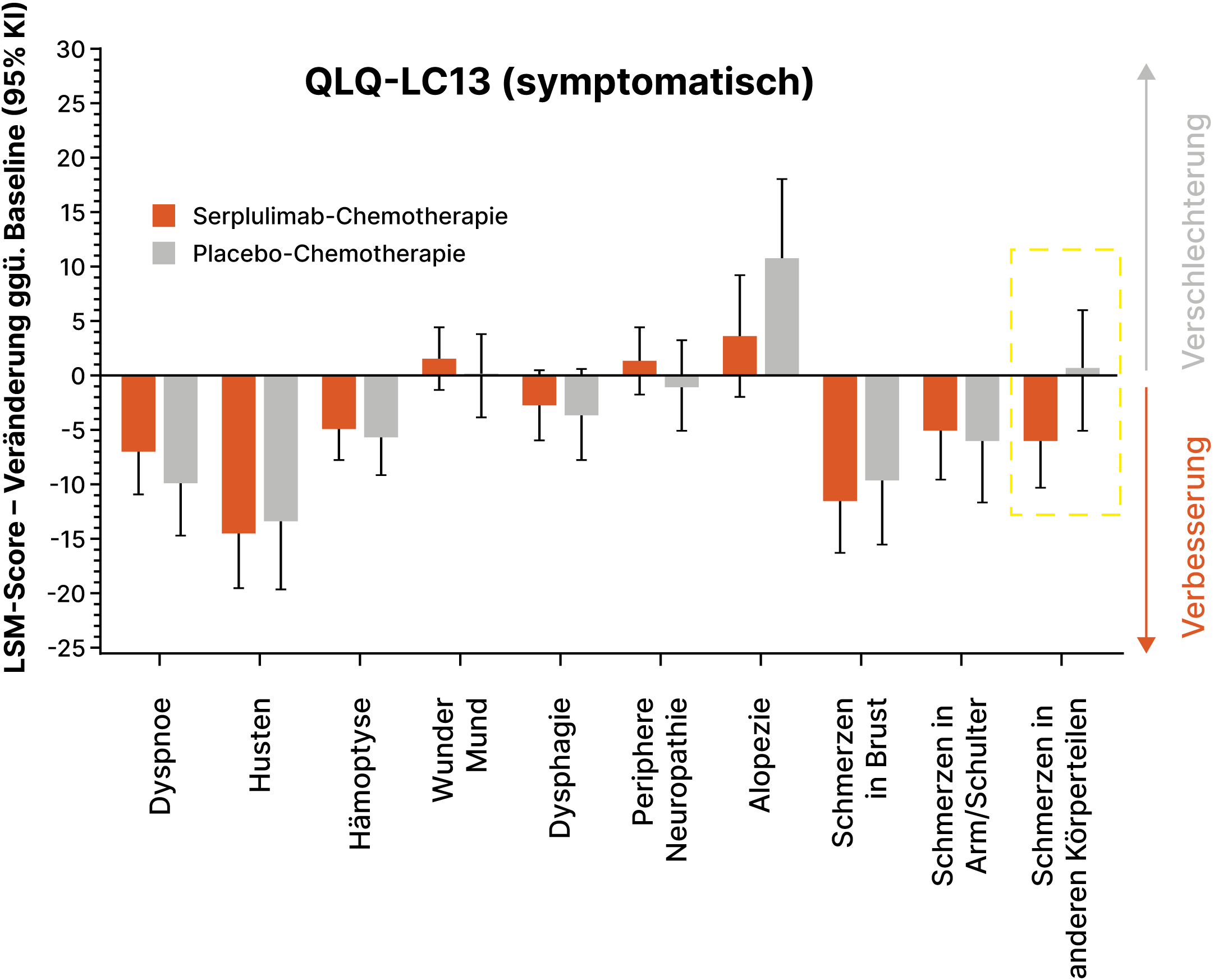
Bewertung der Lebensqualität (Baseline bis Woche 18) anhand des QLQ-LC13-Fragebogenmoduls3
Geschätzte 3-Jahres-Überlebensrate fast 25 %
Die Studie ASTRUM-005 zeigte nach einer medianen Nachbeobachtungszeit von 31,6 Monaten in der Gesamtpopulation (ITT) unter Serplulimab plus Chemotherapie (n = 389) im Vergleich zu Placebo plus Chemotherapie (n = 196) in der Erstlinientherapie folgende Wirksamkeits-Ergebnisse:3
- Die geschätzte 3-Jahres-Überlebensrate lag bei 24,6 % (95 %-Konfidenzintervall [KI]: 19,5-30,1) im Vergleich zu 9,8 % (95 %-KI: 5,6-15,4) im Placebo-Arm.
- Das mediane Gesamtüberleben (OS, primärer Endpunkt) war signifikant länger: 15,8 Monate im Vergleich zu 11,1 Monaten in der Placebo-Gruppe (Hazard Ratio [HR]: 0,61; 95 %-KI: 0,50-0,74).
- Auch das mediane progressionsfreie Überleben (PFS, sekundärer Endpunkt) war signifikant länger: 5,8 Monate im Vergleich zu 4,3 Monate im Placebo-Arm (HR: 0,46; 95 %-KI: 0,38-0,57).
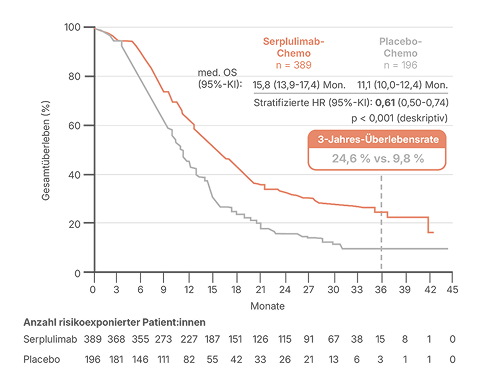
Medianes OS in der Studie ASTRUM-005 (KI: Konfidenzintervall; HR: Hazard Ratio)*, modifiziert nach Cheng Y et al.3
Bekanntes Sicherheitsprofil
Das beobachtete Sicherheitsprofil von Serplulimab war vergleichbar mit jenem anderer Immuntherapien bei fortgeschrittenem SCLC.3 Die Inzidenz und Schweregrade therapieassoziierter unerwünschter Ereignisse (TEAE) waren in beiden Armen vergleichbar.
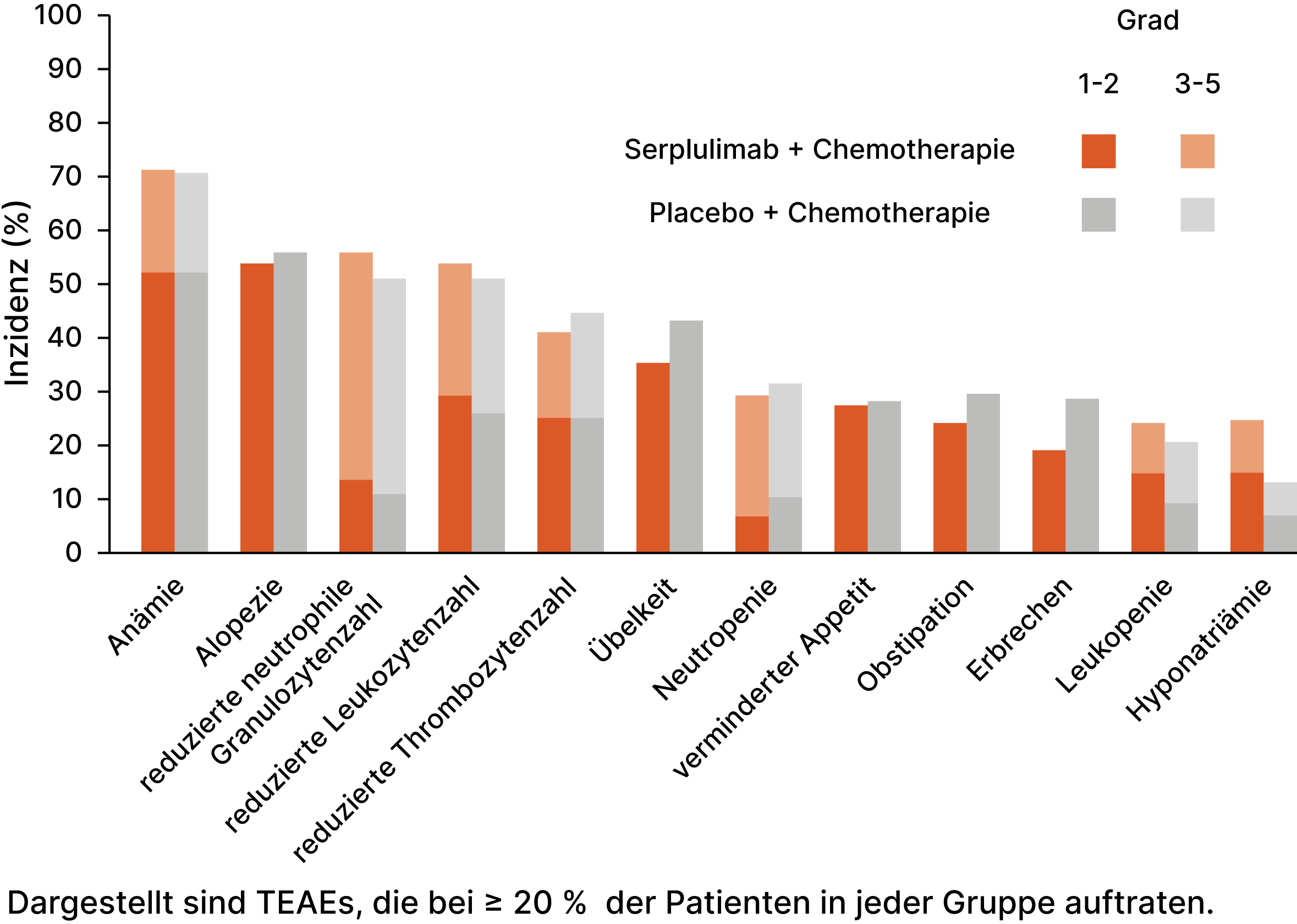
TEAEs der ASTRUM-005-Studie (medianes Follow-up 19,8 Monate), modifiziert nach Cheng Y et al. Dargestellt sind TEAEs, die bei ≥ 20 % der Patient:innen in jeder Gruppe auftraten.4
Pflichttext
1 Fachinformation HETRONIFLY, aktueller Stand.
* Ergebnis der 3. Interimsanalyse der Gesamtpopulation (ITT, Datenschnitt Juni 2023, medianes Follow-up 31,6 Monate) im Rahmen der Studie ASTRUM-005).
2 European Medicines Agency. Hetronifly. https://www.ema.europa.eu/en/medicines/human/EPAR/hetronifly. Letzter Zugriff: Juni 2025.
3 Cheng Y et al. J Clin Oncol 2024; 42 (16 Suppl): Abstract #8100.
4 Cheng Y et al. ESMO Asia 2022; Abstract #LBA9.
|