  |
Liebe Leserinnen und Leser,
bei Patienten# mit allergischem Asthma führt die Inhalation von Allergenen zu einer Überreaktion des Immunsystems, bei der IgE und Zytokine wie IL-4 und IL-13 eine zentrale Rolle spielen.2 Diese Typ-2-Inflammation löst Entzündungskaskaden aus, die zu Bronchialverengung und vermehrter Schleimbildung führen.2
Mit DUPIXENT® die Typ-2-Inflammation präzise bekämpfen*,3
DUPIXENT® adressiert direkt die zugrunde liegende Typ-2-Inflammation, indem es die Signalwege von IL-4 und IL-13 hemmt.3,4
Dies reduziert den IgE-Spiegel im Blut um bis zu 70 % nach 52 Wochen,a,b,1 wie eine Post-hoc-Analyse der QUEST-Studie bei Patienten mit allergischem Asthma und Typ-2-Inflammationc zeigte.
DUPIXENT® kann für Patienten, die nachweislich auf saisonale Allergene reagieren, eine effektive Behandlungsoption während der Allergiesaison bieten.a,d,1,5
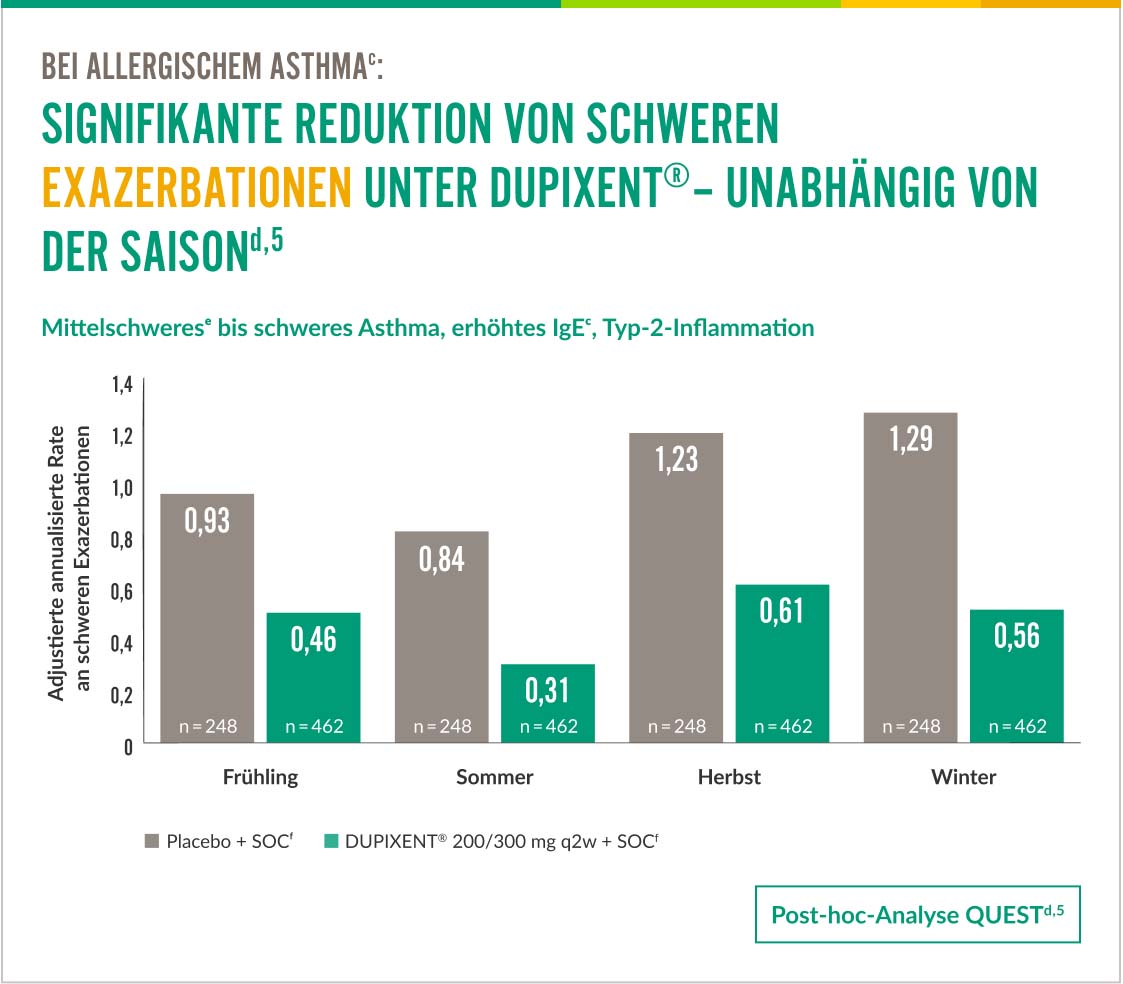
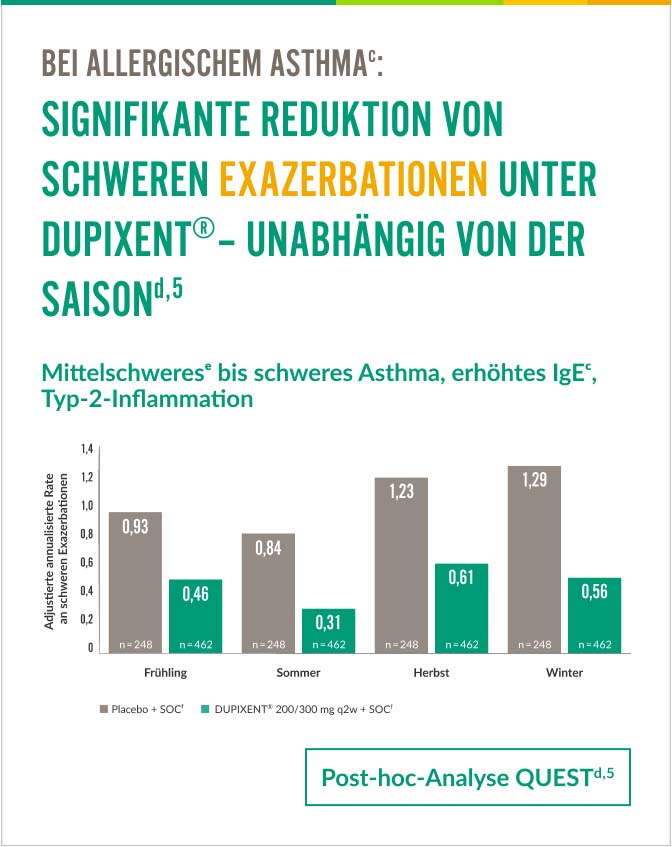
Exazerbationen lassen sich effektiv mindernd,5
Zusätzlich reduzierte DUPIXENT® schwere Exazerbationen bei Patienten mit allergischem Asthma mit Typ-2-Inflammation. Die Reduktion der Exazerbationen zeigte sich ganzjährig über die Allergiesaison hinaus.d,5 |
  |
Erfahren Sie mehr über DUPIXENT® bei allergischem Asthma mit Typ-2-Inflammationc,1,5 und warum die Exazerbationsrate bei schwerem Asthma im Jahresverlauf schwankt.6
|
Zur Allergiesaison gezielt wechseln!
Denken Sie bei allergischem Asthma mit
Typ-2-Inflammation an DUPIXENT®c,1,5 |
|
|
|
  |
Ctrl. = Controller; EOS = eosinophile Granulozyten; FeNO = fraktioniertes exhaliertes Stickstoffmonoxid (NO); ICS = inhalative Kortikosteroide; IgE = Immunglobulin E; IL = Interleukin; kU = kilo Units; ppb = parts per billion; q2w = einmal alle zwei Wochen; SOC = standard of care.
* DUPIXENT® ist zugelassen als Add-on-Erhaltungstherapie bei Erwachsenen und Jugendlichen ab 12 Jahren mit schwerem Asthma mit Typ-2-Inflammation gekennzeichnet durch eine erhöhte Anzahl der Eosinophilen im Blut (≥ 150/μl) und/oder erhöhtes FeNO (≥ 25 ppb), das trotz hochdosierter inhalativer Kortikosteroide (ICS) plus einem weiteren zur Erhaltungstherapie angewendeten Arzneimittel unzureichend kontrolliert ist. DUPIXENT® ist zugelassen als Add-on-Erhaltungstherapie bei Kindern von 6 bis 11 Jahren mit schwerem Asthma mit Typ‑2-Inflammation gekennzeichnet durch eine erhöhte Anzahl der Eosinophilen im Blut (≥ 150/μl) und/oder erhöhtes FeNO (≥ 20 ppb), das trotz mittel- bis hochdosierter ICS plus einem weiteren zur Erhaltungstherapie angewendeten Arzneimittel unzureichend kontrolliert ist.3 | # Allein aus Gründen der besseren Lesbarkeit wurde auf die gleichzeitige Verwendung geschlechtsspezifischer Sprachformen verzichtet. Sämtliche Personenbezeichnungen gelten aber selbstverständlich für alle Geschlechter. | a Corren et al.1 ist eine Post-hoc-Analyse der QUEST-Studie7: Die QUEST-Studie war eine 52-wöchige, randomisierte, doppelt verblindete, placebokontrollierte Parallelgruppenstudie mit Patienten (n = 1.902) mit mittelschwerem bis schwerem Asthma, die zu Beginn der Studie (Baseline) mittel- (48,5 %)g oder hochdos. (51,5 %) ICS und mindestens einen Controller erhielten. In der Post-hoc-Analyse von Corren et al. wurden zwei Gruppen miteinander verglichen: Patienten mit allergischem Asthma (n = 1.083; bei Studienbeginn: Gesamt-IgE ≥ 30 IE/ml und IgE ≥ 0,35 kU/l gegen mindestens ein ganzjährig auftretendes Aeroallergenh) und ohne allergisches Asthma (n = 819). Die Studie war nicht speziell für die Analyse der Unterschiede in den Subgruppen allerg. Asthma/nicht allerg. Asthma gepowert. | b Reduktion des medianen Gesamt-IgEs von 304 IE/ml auf ca. 90 IE/ml in Woche 52 unter Dupilumab 200 mg q2w bei Patienten mit mittel-g oder hochdosiert. ICS + Ctrl. und mit Gesamt-IgE ≥ 30 IE/ml und IgE ≥ 0,35 kU/l gegen mindestens ein ganzjährig auftretendes Aeroallergenh bei Studienbeginn1 | c Bei Studienbeginn: Gesamt-IgE ≥ 30 IE/ml und IgE ≥ 0,35 kU/l gegen mindestens ein ganzjährig auftretendes Aeroallergenh | d Peters et al.5 ist eine Post-hoc-Analyse der QUEST-Studie7: Die QUEST-Studie war eine 52-wöchige, randomisierte, doppelt verblindete, placebokontrollierte Parallelgruppenstudie mit Patienten (n = 1.902) mit mittelschwerem bis schwerem Asthma, die zu Beginn der Studie (Baseline) mittel- (48,5 %)g oder hochdos.
(51,5 %) ICS und mindestens einen Controller erhielten. In der Post-hoc-Analyse von Peters et al. wurden zwei Gruppen miteinander verglichen: Patienten mit allergischem Asthma (n = 710; bei Studienbeginn: Gesamt-IgE ≥ 30 IE/ml und IgE ≥ 0,35 kU/l gegen mindestens ein ganzjährig auftretendes Aeroallergenh) und ohne allergisches Asthma (n = 517). Die Studie war nicht speziell für die Analyse der Unterschiede in den Subgruppen allerg. Asthma/nicht allerg. Asthma gepowert. | e DUPIXENT® ist in Deutschland nicht zur Therapie mittelschweren Asthmas zugelassen. | f Mittel-g bis hochdosierte ICS + zweiten Controller ± dritten Controller7 | g Für Patienten ab 12 Jahren, die mit mitteldosiertem ICS behandelt werden, ist DUPIXENT® in Deutschland nicht zugelassen. | h Die folgenden ganzjährigen Allergene wurden berücksichtigt: Dermatophagoides farinae, Dermatophagoides pteronyssinus, Alternaria alternata, Cladosporium herbarum, Katzen- und Hundehaare, Küchenschabe (Blatella germanica), Orientalische Schabe (Blatta orientalis) und Aspergillus fumigatus.
1. Corren J et al. J Allergy Clin Immunol Pract 2020; 8(2): 516–526; 2. Komlósi ZI et al. Mol Aspects Med 2022; 85: 100995; 3. DUPIXENT® Fachinformationen, aktueller Stand; 4. Gandhi NA et al. Nat Rev Drug Discov 2016; 15(1): 35–50; 5. Peters AT et al. Ann Allergy Asthma Immunol 2024; 132(4): 477–484; 6. Ramsahai JM et al. Am J Respir Crit Care Med 2019; 199(4): 423-432; 7. Castro M et al. N Engl J Med 2018; 378(26): 2486–2496. |
|
|
 |
MAT-DE-2500471-1.0-02/2025
© Sanofi 2025. Alle Rechte vorbehalten
Datenschutz | Nutzungsbedingungen | Kontakt | Impressum
Sanofi-Aventis Deutschland GmbH · Industriepark Höchst, K703 · D-65926 Frankfurt am Main
Telefon +49 (0) 69 305 80710 · www.sanofi.de
Sitz der Gesellschaft: Frankfurt am Main – Handelsregister: Frankfurt am Main, Abt. B Nr. 40661
Vorsitzender des Aufsichtsrates: Brendan O’Callaghan – Geschäftsführer: Heidrun Irschik-Hadjieff (Vorsitzende), Oliver Coenenberg, Dr. Peter Naumann, Anne Reuschenbach, Dr. Marion Zerlin
|
|
|
|
|
„Kompakt Pneumologie“ ist ein Titel der Biermann Verlag GmbH in Köln. Sie erhalten diese E-Mail, da Sie für diesen Newsletter angemeldet sind. Sie können in unserem Fachportal weitere Newsletter zu verschiedenen medizinischen Fachrichtungen abonnieren. Sollten Sie kein Interesse mehr an diesem Newsletter haben, können Sie sich hier abmelden. Haben Sie Fragen oder Anregungen zu unseren Themen und Inhalten, freuen wir uns auf Ihre E-Mail: [email protected]. Bitte beachten Sie, dass dieser Newsletter nur Angehörigen der Heilberufe gemäß HWG §10 zugänglich gemacht werden darf; das gilt auch für das Weiterempfehlen und Weiterleiten.
Impressum: Biermann Verlag GmbH | MedCon Health Contents GmbH | HRB Bonn 11110 | HRB Köln 78926
Geschäftsführer: Dr. med. Hans Biermann
Hier vollständiges Impressum aufrufen
|
|
|
|
|
|