|
ObgemsaTM: Neu und unkompliziert bei überaktiver Blase
Im Alter von 40 bis 79 Jahren sind in Deutschland 9 bis 14 % der Frauen von einer überaktiven Blase betroffen, ab 80 Jahren steigt der Anteil auf 33 %.1 Bei Männern liegt der Anteil über alle Altersgruppen Schätzungen zufolge bei 4 bis 8 %.2 Eine überaktive Blase kann die Lebensqualität Betroffener deutlich beeinträchtigen.1 Mit ObgemsaTM ist seit Juni 2024 nun auch in Europa ein neuartiger, hochselektiver und potenter β3-Agonist zur symptomatischen Behandlung der überaktiven Blase bei Erwachsenen zugelassen, der seit 1. Oktober 2024 in Deutschland verordnet werden kann.3 Eine breite Evidenz untermauert das Wirksamkeits- und Sicherheitsprofil unter Studien- und Alltagsbedingungen.4,5,6 Darüber hinaus liegen zu ObgemsaTM in den USA, Japan und Südkorea bereits langjährige Erfahrungen vor.7,8,a
Zulassungsstudie zeigte überlegenes Sicherheitsprofil bei guter Therapietreue
Die Zulassung von ObgemsaTM erfolgte u. a. auf Basis der Ergebnisse der doppelblinden Phase-III-Studie EMPOWUR.4 Im Rahmen der Studie wurden 1.518 Erwachsene mit einer überaktiven Blase und 8 oder mehr Miktionen pro Tag 5:5:4 auf ObgemsaTM 75 mg, Placebo bzw. Tolterodin 4 mg mit verzögerter Freisetzung (aktive Kontrolle) randomisiert. Die Ergebnisse zeigten eine Wirksamkeit von ObgemsaTM auf die Kernsymptome der überaktiven Blase. So wurde in Woche 12 eine Abnahme der Miktionen um durchschnittlich 1,8 unter ObgemsaTM beobachtet (p < 0,001 vs. Placebo, co-primärer Endpunkt), um 1,3 unter Placebo und um 1,6 unter Tolterodin (p = 0,0988 vs. Placebo). Dranginkontinenz-Episoden sanken um durchschnittlich 2,0 unter ObgemsaTM (p < 0,0001 vs. Placebo, co-primärer Endpunkt), 1,4 unter Placebo und 1,8 unter Tolterodin (p = 0,0123 vs. Placebo; Abb. 1).4 Bei 41 % der Patienten unter ObgemsaTM wurde überdies zu Woche 52 eine komplette Abwesenheit von Dranginkontinenz-Episoden erreicht, bei 61 % der Teilnehmenden wurde eine Reduktion um mindestens 75 % beobachtet.9
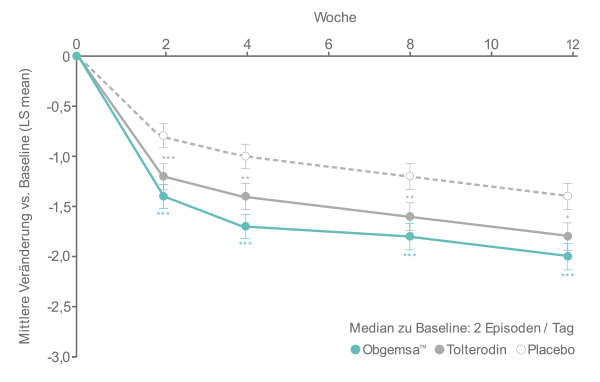
Abb. 1 Anzahl der täglichen Dranginkontinenz-Episoden unter ObgemsaTM, Tolterodin und Placebo (mod. nach Staskin D et al. 20204)
Das kardiovaskuläre Risiko erwies sich dabei als günstig, das Sicherheitsprofil von ObgemsaTM war generell vergleichbar mit Placebo. Schwerwiegende unerwünschte Nebenwirkungen wurden bei 1,5 % der Patienten unter ObgemsaTM beobachtet vs. 1,1 % unter Placebo. Dabei war die Therapietreue hoch: Die Therapieabbruchrate aufgrund von unerwünschten Arzneimittelwirkungen unter ObgemsaTM lag bei < 2 %.4
Keine Dosisanpassung bei Vorbelastungen und einfache Einnahme
Ergebnisse der Studie AMBULATORY zeigten überdies keinen klinisch relevanten oder statistisch signifikanten Einfluss auf Blutdruck oder Herzfrequenz.10 Bei kardiovaskulären Vorerkrankungen wie Hypertonie, erhöhter Herzfrequenz, leichter, mittlerer oder schwerer Nierenfunktionsstörung (15 ml/min < GFR < 90 ml/min und nicht dialysepflichtig) sowie leichter bis mittelschwerer Leberfunktionsstörung (Child-Pugh A und B) ist bei ObgemsaTM als erstem und einzigem β3-Agonist keine Dosisanpassung nötig.3,10 Eine Co-Medikation mit starken und moderaten CYP3A-Inhibitoren / -Induktoren sowie P-gp-Inhibitoren / -Induktoren ist überdies möglich. CYP2D6-Interaktionen bestehen ebenfalls nicht. ObgemsaTM wird als Einheitsdosis eingenommen. Die Tablette ist zudem mörserbar und sollte danach unverzüglich mit etwas Nahrung und einem Glas Wasser eingenommen werden.3
a. Zulassung in Japan: 2018, Südkorea: 2022, USA: 2020
1. Schreiber Pedersen L et al. Prevalence of urinary incontinence among women and analysis of potential risk factors in Germany and Denmark. Acta Obstet Gynecol Scand. 2017 Aug;96(8):939-948.
2. Stiftung Gesundheitswissen. Dranginkontinenz. https://www.stiftung-gesundheitswissen.de/wissen/dranginkontinenz/hintergrund. Accessed: 29.08.2024.
3. Fachinformation Obgemsa, 06/24.
4. Staskin D et al. International Phase III, Randomized, Double-Blind, Placebo and Active Controlled Study to Evaluate the Safety and Efficacy of Vibegron in Patients with Symptoms of Overactive Bladder: EMPOWUR. J Urol. 2020 Aug;204(2):316-324.
5. Kennelly M et al. Long-term efficacy and safety of vibegron versus mirabegron and anticholinergics for overactive bladder: a systematic review and network meta-analysis.
6. Chastek B et al. Real-World Adherence to and Persistence with Vibegron in Patients with Overactive Bladder: A Retrospective Claims Analysis. Adv Ther. 2024 May;41(5):2086-2097.
7. FDA Drug Trial Snapshot: Gemtesa. https://www.fda.gov/drugs/drug-approvals-and-databases/drug-trials-snapshot-gemtesa. Accessed: 12.06.2024.
8. CHMP-Statement, Pierre Fabre Pharma. Data on file, April 2024.
9. Staskin D et al. Once-Daily Vibegron 75 mg for Overactive Bladder: Long-Term Safety and Efficacy from a Double-Blind Extension Study of the International Phase 3 Trial (EMPOWUR). J Urol. 2021 May;205(5):1421-1429.
10. Weber MA et al. Effects of vibegron on ambulatory blood pressure in patients with overactive bladder: results from a double-blind, placebo controlled trial. Blood Pressure Monitoring 2022;27(2):128-134.
Pflichtangaben
Obgemsa 75 mg Filmtabletten
Wirkst.: Vibegron. Zus.: 1 Filmtablette enthält 75 mg Vibegron. Sonst. Bestandteile mit bekannter Wirkung: 1,5 mg Lactose. Sonstige Bestandteile: Tablettenkern: Mannitol, mikrokristalline Cellulose, Croscarmellose-Natrium, Hydroxypropylcellulose, Magnesiumstearat. Filmüberzug: Indigokarmin-Aluminiumsalz (E132), Hypromellose (E464), Eisen(III)-hydroxid-oxid x H2O (E172), Lactose-Monohydrat, Titandioxid (E171), Triacetin. Anwend.: Bei Erw. zur symptomat. Therapie bei überaktiver Blase (ÜAB-Syndrom). Gegenanz.: Überempfindlichkeit gegen Inhaltstoffe. Nebenw.: Häufig: Kopfschmerzen, Obstipation, Diarrhoe, Übelkeit, Harnwegsinfektion, Restharn erhöht. Gelegentl.: Hitzewallung, Ausschlag (einschließlich Ausschlag mit Juckreiz und erythematöser Hautausschlag), Harnverhalt (einschließlich Anstrengen beim Wasserlassen). Warnhinw.: enthält Lactose. Verschreibungspflichtig. Weitere Hinweise: siehe Fachinformation. Stand: Juni 2024. Pierre Fabre Pharma GmbH, Neuer Messplatz 5, 79108 Freiburg
DE-OBS-09-24-2400008
|